Halogen
| Skupina 17 v periodnem sistemu | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||
| ↓ Perioda | |||||||||||
| 2 | Fluor (F) 9 Halogen | ||||||||||
| 3 | Klor (Cl) 17 Halogen | ||||||||||
| 4 | Brom (Br) 35 Halogen | ||||||||||
| 5 | Jod (I) 53 Halogen | ||||||||||
| 6 | Astat (At) 85 Halogen | ||||||||||
| 7 | Tenes (Ts) 117 Halogen | ||||||||||
|
Legenda
| |||||||||||

Halogeni ali halogeni elementi so skupina nekovin, ki tvorijo 17. (bivšo VII oziroma VIIA) skupino periodnega sistema elementov. Mednje spadajo fluor (F), klor (Cl), brom (Br), jod (I), astat (At) in ununseptij (Uus). Skupina je poznana tudi kot fluorova skupina.
Nastanek imen
[uredi | uredi kodo]Naziv halogen se je prvič pojavil v osemnajstem stoletju v francoski znanstveni literaturi. Beseda je nastala iz grških besed hals (morje) in halas (sol) in pripone –gen (generirati, tvoriti). Izraz halogen torej pomeni element, ki (s kovinami) tvori soli.
Ime fluor je nastalo iz latinske besede fluere, ki pomeni "pretakati se", klor iz grške besede χλωρóς (hlôros), ki pomeni "svetlozelen", brom iz grške besede βρῶμος (brómos), ki pomeni "smrdi (po kozah)", jod iz grške besede ιώδης (iodes), ki pomeni "vijoličast" in astat iz grške besede άσταζής (astathes), ki pomeni "nestalen".
Nahajališča
[uredi | uredi kodo]
Halogeni elementi so zelo reaktivni, zato jih v naravi najdemo samo v spojinah ali v ionski obliki. Halogenidne ione in oksoanione, na primer jodatni ion IO−3, najdemo v mnogih mineralih in v morski vodi. Halogenirane organske spojine so sestavine nekaterih naravnih snovi v živih organizmih.
Astat najdemo v naravi v neznatnih količinah kot nestalni produkt radioaktivnega razpada urana, astato-urana in torija.[1]
Fizikalne lastnosti
[uredi | uredi kodo]Halogeni so edina skupina elementov, ki imajo pri normalnih pogojih predstavnike v vseh treh agregatnih stanjih: fluor je temno rumen plin (temno rumen samo v tekočem stanju) , klor je rumenozelen plin, brom je pri sobni temperaturi temno rjava tekočina, jod pa je sivočrna trdna snov s kovinskim sijajem. Astat je radioaktiven.
Halogeni kažejo po skupini navzdol številne trende: elektronegativnost in reaktivnost po skupini padata, gostota, temperature tališč in vrelišč pa naraščajo.
| Element | Standardna atomska masa | Tališče (K) | Vrelišče (K) | Elektronegativnost po Paulingu |
|---|---|---|---|---|
| Fluor | 18,998 | 53,53 | 85,03 | 3,98 |
| Klor | 35,453 | 171,60 | 239,11 | 3,16 |
| Brom | 79,904 | 265,80 | 332,00 | 2,96 |
| Jod | 126,904 | 386,85 | 457,40 | 2,66 |
| Astat | 210 | 575 | 610 | 2,20 |
Halogeni elementi imajo na zunanji orbitali po sedem elektronov, ki odločilno vplivajo na njihove kemijske lastnosti. Zaradi velike reaktivnosti so kot elementi obstojni samo v dvoatomskih molekulah. Značilnosti njihovih dvoatomnih molekul so prikazane v naslednji tabeli:
| Element | Molekula | Zgradba | Model | d(X−X) [pm] (plinast) |
d(X−X) [pm] (trden) |
|---|---|---|---|---|---|
| Fluor | F2 | 143 | 149 | ||
| Klor | Cl2 | 199 | 198 | ||
| Brom | Br2 | 
|
228 | 227 | |
| Jod | I2 | 
|
266 | 272 |
Vez v molekulah je nepolarna enojna kovalentna vez. Zaradi nepolarne vezi so halogeni slabo topni v vodi, dobro pa se raztapljajo v nepolarnih topilih. Vodne raztopine klora (klorovica), joda (jodovica) in broma (bromovica) se uporabljajo v analizni kemiji.
Kemijske lastnosti
[uredi | uredi kodo]Reaktivnost
[uredi | uredi kodo]Halogeni so zelo reaktivni in kot taki škodljivi in v večjih količinah smrtno nevarni za žive organizme. Njihova reaktivnost je posledica sedmih elektronov na zunanji orbitali, kar pomeni, da jim do popolne zgradbe zunanje orbitale manjka samo en elektron. Manjkajoči elektron dobijo s kemijsko reakcijo z drugimi elementi.
Fluor je najbolj elektronegativen element in spada med najbolj reaktivne elemente. Najeda tudi zelo inernetne snovi, na primer steklo, ker v prisotnosti že zelo majhne količine vode tvori silicijev tetrafluurid (SiF4). Steklena laboratorijska posoda za shranjevanje fluora mora biti zato popolnoma suha ali izdelana iz teflona, bakra, niklja ali jekla. Fluor namreč na kovinskih površinah tvori zaščitni sloj obstojnih kovinskih fluoridov. Fluor je zelo strupen in se spaja celo s težjimi žlahtnimi plini.
Klor in jod ubijata potencialno škodljive mikroorganizme in se zato uporabljata za dezinfekcijo pitne vode, plavalnih bazenov, svežih ran in kože (jod) in posode. Klor se kot natrijev hipoklorit (NaOCl, po domače varikina) uporablja tudi za beljenje tkanin, celuloze in papirja.
Raztapljanje v vodi
[uredi | uredi kodo]Fluor zelo burno reagira z vodo, pri čemer nastajata kisik (O2) in vodikov fluorid (HF):[2]
- 2 F2(g) + 2 H2O(l) → O2(g) + 4 HF(aq)
Klor je v vodi slabo topen. Njegova maksimalna topnost je približno 1 % (pri temperaturi 9,6 °C).[3] Raztopljeni klor tvori zmes klorovodikove kisline (HCl) in hipoklorove kisline (HClO) in je primeren za dezinfekcijsko sredstvo ali sredstvo za beljenje:
- Cl2(g) + H2O(l) → HCl(aq) + HClO(aq)
Topnost broma je 3,41 g/100 g vode (pri 20 °C)[4] Z vodo reagira podobno kot klor in tvori vodikov bromid (HBr) in hipobromovo kislino (HbrO), vendar reakcija poteka počasneje:
- Br2(g) + H2O(l) → HBr(g) + HBrO(aq)
Topnost joda v vodi je zelo majhna (0,03 g/100 g vode pri 20 °C) in z vodo ne reagira.[5] Jod se dobro raztaplja v vodni raztopini jodidnih ionov (I-), ker z njimi tvori trijodidne ione (I3-).
Reakcije s kovinami
[uredi | uredi kodo]Halogeni reagirajo s kovinami in tvorijo soli – od tod tudi njihovo ime. Reakcije s kovinami iz prve in druge skupine elementov so zelo burne, gorijo pa tudi kovine z desne polovice periodnega sistema, na primer arzen, antimon in bizmut, ki spadajo v 15. (bivša VA) skupino elementov periodnega sistema.[1] V reakcijah se sproščata toplota in svetloba.
- 2 Na(s) + Cl2(g) → 2 NaCl
Reakcije z vodikom
[uredi | uredi kodo]Halogeni reagirajo z vodikom in tvorijo vodikove halogenide. Reakcije so burne in celo eksplozivne:[1]
- H2 + Cl2 → 2 HCl
Vodne raztopine vodikovih halogenidov, razen HF, so močne kisline.
Spojine
[uredi | uredi kodo]Vodikovi halogenidi
[uredi | uredi kodo]Vsi halogeni tvorijo z vodikom binarne spojine vodikove halogenide: HF, HCl, HBr, HI in HAt, katerih vodne raztopine so, razen HF, močne kisline. Astatovodikove kisline (HAt) se običajno ne uvršča med halogenvodikove kisline, ker je zaradi ekstremne nestabilnosti astata zaradi razpada alfa tudi sama izredno nestabilna.
Okso kisline
[uredi | uredi kodo]Halogeni elementi, razen floura, tvorijo naslednje vrste kislin:
- HXO: npr. HClO, klorova(I) kislina, hipoklorasta kislina
- HXO2: npr. HClO2, klorova(III) kislina, klorasta kislina
- HXO3: npr. HClO3, klorova(V) kislina, klorova kislina
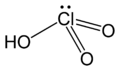
- HXO4: npr. HClO4, klorova(VII) kislina, perklorova kislina
Kisline imajo naslednje strukture:
-
Hipoklorasta kislina
-
Klorasta kislina
-
Klorova kislina
-
Perklorova kislina
Interhalogene spojine
[uredi | uredi kodo]Halogeni elementi med seboj reagirajo in tvorijo interhalogene spojine. Dvoatomne spojine, na primer BrF, ICl in ClF se v nekaterih primerih obnašajo kot čisti halogeni, v nekaterih primerih so njihove lastnosti nekje med lastnostmi njihovih starševskih elementov, v nekaterih primerih pa so v njihovem popolnem nasprotju: Cl2 in I2 sta, na primer, topna v nepolarnem topilu CCl4, ICl pa ne, ker je zaradi razlike v elektronegativnosti Cl2 in I2 molekula ICl polarna.
Halogenirane organske spojine
[uredi | uredi kodo]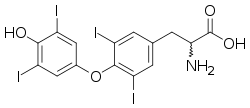
Halogenirane organske spojine (organski halogenidi) so v naravi bolj redke, v sintetskih organskih spojinah pa so kar dobro zastopane, predvsem med organskimi topili in plastičnimi masami (PVC, PTFE). Najpogostejši halogen je klor, ki se kot kloridni ion Cl− nahaja tudi v človeškem organizmu. Največ ga je v želodčni kislini (kot HCl) in v možganih, v katerih igra ključno vlogo pri delovanju inhibitornih nevrotransmiterjev GABA (derivati gama-aminomaslene kisline). Jod je v sledovih potreben za tvorbo hormonov ščitnice, na primer tiroksina. Fluor in brom za človeški organizem nista esencialna elementa, čeprav majhne količine fluora ugodno vplivajo na odpornost zobne sklenine.
Polihalogenirane spojine
[uredi | uredi kodo]Polihalogenirane spojine so umetno proizvodene spojine z več substituiranimi halogeni, ki imajo zelo široke možnosti uporabe. Mnoge spojine so kancerogene in se akumulirajo v organizmih. Najbolj škodljive spojine so PCB (poliklorirani bifenili), PBDE (polibromirani difenil etri) in PFC (perfluorirane spojine), obstoja pa še mnogo drugih.
Reference
[uredi | uredi kodo]- ↑ 1,0 1,1 1,2 Egon Wiberg, Anorganska kemija, ŠK, Zagreb (1967), str. 89-150
- ↑ The Oxidising Ability of the Group 7 Elements
- ↑ »Solubility of chlorine in water«. Arhivirano iz prvotnega spletišča dne 23. aprila 2012. Pridobljeno 17. februarja 2009.
- ↑ »Properties of bromine«. Arhivirano iz prvotnega spletišča dne 8. decembra 2007. Pridobljeno 17. februarja 2009.
- ↑ Iodine MSDS