Fenilalanin
 L-fenilalanin
| |
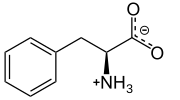 L-fvenilalanin pri fiziološkem pH
| |
| Imena | |
|---|---|
| IUPAC ime
fenilalanin
| |
| Druga imena
2-amino-3-fenilpropanojska kislina
| |
| Identifikatorji | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.517 |
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| Lastnosti | |
| C6H5CH2CH(NH2)COOH | |
| Kislost (pKa) | 1.83 (carboxyl), 9.13 (amino) |
| Nevarnosti | |
| NFPA 704 (diamant ognja) | |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Fenilalanin (skrajšano Phe ali F) [2] je α - aminokislina s formulo C6H5CH2CH(NH2)COOH. Razumeti jo je mogoče kot alanin, v katerem je benzil skupina nadomeščena z metilno skupino, podobno kot pri alaninu, kjer je terminalni vodik zamenjan s fenil skupino. Ta esencialna aminokislina je zaradi inertne hidrofobne narave stranske benzil verige razvrščena med nevtralne, nepolarne aminokisline. Levo sučni (L) izomer spojine se vgrajuje v proteine, kot to kodira DNA. Kodona za L-fenilalanin sta UUU in UUC. Fenilalanin je prekurzor za tirozin, za nevrotransmiterje dopamin, noradrenalin in adrenalin in za kožni pigment melanin.
Fenilalanin je najti v materinem mleku sesalcev. Uporablja se v proizvodnji hrane in pijač in prodaja kot dodatek prehrani zaradi njegovih domnevnih analgetičnih in antidepresivnih učinkov. Je neposreden predhodnik za pogosto uporabljeno prehransko dopolnilo, nevromodulator feniletilamin.
Fenilalanin je esencialna aminokislina, ki je ljudje in druge živali ne morejo sintetizirati - potrebujejo hrano, ki vsebuje fenilalanin oziroma proteine, ki to aminokislino vsebujejo.
Zgodovina[uredi | uredi kodo]
Prva sta fenilalanin opisala 1879 Schulze in Barbieri, ko sta v sadikah rastline rumeni volčji bob ( Lupinus luteus) identificirala spojino z empirično formulo C 9 H 11 NO 2, . Erlenmeyer in Lipp sta kot prva leta 1882 fenilalanin sintetizirala iz fenilacetaldehida, cianovodika in amoniaka.[3] [4] [3]
Genetski kodon za fenilalanin sta odkrila J. Heinrich Matthaei in Marshall W. Nirenberg leta 1961. Dokazala sta, da mRNK, sestavljen iz zaporedja ene in iste snovi, uracila, v E. coli povzroči izdelavo polipeptidov iz ene same aminokisline, to je fenilalanina. To odkritje je pomagalo razgonetiti metodo, ki celicam omogoča v genomu zapisano informacijo prepisovati v proteine.
Viri v prehrani[uredi | uredi kodo]
Dobri viri fenilalanina so jajca, kurje meso, jetra, govedina, mleko in soja.[5] Drugi viri so med drugim špinača in listnata zelenjava, tofu, listi amaranta in bobova zrna.
Druge biološke vloge[uredi | uredi kodo]
L-fenilalanin se biološko pretvarja v L-tirozin, eno od aminokislin, ki jih kodira DNK. L-tirozin se nato pretvori v L-DOPA, ta pa dalje v dopamin, noradrenalin in adrenalin. Slednje tri snovi so znane pod imenom kateholamini.
Fenilalanin uporablja za aktivni transport skozi pregrado kri-možgani isti kanal kot triptofan. V prevelikih količinah lahko nadomeščanje moti proizvodnjo serotonina in drugih aromatskih aminokislin in pa dušikovega oksida zaradi prekomerne porabe (in sčasoma padajoče razpoložljivosti) s tem povezanih kofaktorjev, železa ali tetrahidrobiopterina. Fenilalanin, ki ga je najti v sintetični kemikaliji aspartamu (nadomestku za sladkorja) lahko kot delež v visokih odmerkih aspartama včasih povzroči napade; za to teorijo je malo dokazov in tveganje je majhno.[6] Ustrezni encimi za te spojine so družina hidroksilaz za aromatične aminokisline in sintaza dušikovega oksida. V rastlinah je fenilalanin izhodna spojina za sintezo flavonoidov. Lignan se tvori iz fenilalanina in iz tirozina. Encim fenilalanin-amonia-liaza pretvarja fenilalanin v cinamsko kislino[9]
Fenilketonurija[uredi | uredi kodo]
Genetska motnja fenilketonurija (PKU) ima posledico, da organizem ni zmožen presnavljati fenilalanin, ker mu manjka encim fenilalanin hidroksilaza. Osebe s to motnjo so znane pod imenom "fenilketonuretiki" in morajo vnos fenilalanina nadzorovati. Redka "variantna oblika" fenilketonurije je tako imenovana hiperfenilalaninemija, katere vzrok je nezmožnost sintetizirati kofaktor tetrahidrobiopterin, ki ga je mogoče dopolniti. Nosečnice s hiperfenilalaninemijo lahko kažejo podobne motnje (visoke ravni fenilalanina v krvi), vendar simptomi po navadi izginejo ob koncu nosečnosti. Nosečnice s fenilketonurijo morajo paziti na ravni fenilalanina v svoji krvi, tudi če je plod za gensko napako heterozigoten, ker jetrna nezrelost na zarodek bi lahko negativno vpliva. Ljudje, ki fenilalanina ne morejo presnavljati, morajo svoj vnos beljakovin nadzorovati, da med razgrajevanjem beljakovin v aminokisline ne pride do kopičenja fenilalanina.
Fenilketonuriki pogosto uporabljajo krvne preiskave za spremljanje količine fenilalanina v krvi. Rezultati laboratorijskih testov za ravni fenilalanina lahko da uporabljajo različne enote, med drugim mg / dl in mol / L. Ena mg / dl fenilalanina ustreza približno 60 mol / L.
Vir neživilskega fenilalanina je umetno sladilo aspartam. Ta spojina, ki se prodaja pod trgovskima imenoma Equal in NutraSweet, se presnavlja v telesu v več kemičnih stranskih proizvodov, med drugim v fenilalanin. Osebe s fenilketonurijo, ki imajo težave pri razgradnji beljakovin in spremljajočem kopičenju fenilalanina v telesu, iimajo lahko tudi probleme pri uživanju aspartama, čeprav v manjši meri. Zato morajo v Avstraliji, ZDA in Kanadi vsi izdelki, ki vsebujejo aspartam, nositi oznako: "Fenilketonuretiki: Vsebuje fenilalanin." V Veliki Britaniji morajo živila, ki vsebujejo aspartam, imeti nalepko s seznamom sestavin, kjer je navedena prisotnost "aspartama ali E951" [7] in označena morajo z opozorilom "Vsebuje vir fenilalanina." Tudi v Braziliji je za izdelke, ki vsebujejo fenilalanin, obvezna oznaka "Contém Fenilalanina" (to je portugalščini "vsebuje fenilalanin"). Ta opozorila so v pomoč osebam z diagnozo fenilketonurije, da se jim ob nabavljanju hrane lahko izognejo.
Genetiki so pred kratkim sekvencirali genom opic makaki. Njihove raziskave so našli "nekaj primerov za običajno oblika beljakovine, ki je podobna obolelemu proteinu pri ljudeh", vključno z markerji za fenilketonurijo.[8]
D-, L- in DL-fenilalanin[uredi | uredi kodo]
Stereoizomerni D-fenilalanin (DPA) se pridobiva s konvencionalno organsko sintezo, bodisi kot enantiomer ali kot sestavina racemične zmesi. V biosintezi beljakovin ni udeležen, četudi so zanj dokazali prisotnost majhnih količinah v proteinih - zlasti v starih beljakovinah in v predelanih prehrambnih proteinih. Biološke funkcije D-aminokislin ostajajo nepojasnjene, čeprav je D-fenilalanin farmakološko aktiven za niacin receptor 2.[9]
DL-fenilalanin (DLPA) se prodaja kot dodatek prehrani zaradi njegovih domnevnih analgetskih in antidepresivnih učinkov. DL-fenilalanin je zmes D-fenilalanina and L-fenilalanina. Cenjena analgetična dejavnost DL-fenilalanina naj bi bila posledica zavirajočega vpliva D-fenilalanina na encim karboksipeptidaza A, ki razgrajuje enkephalin.[10] Mehanizem, po katerem naj bi DL fenilalanin deloval antidepresivno, je mogoče razložiti z vlogo L-fenilalanina v sintezi predhodnikov za nevrotransmiterja noradrenalin in dopamin. Zvišane ravni noradrenalina in dopamina v možganih naj bi imele antidepresivni učinek. D-fenilalanin se absorbira iz tankega črevesa in prenaša v jetra preko portalnega obtoka. Majhna količina D-fenilalanina se zgleda pretvori v L-fenilalanin. D -fenilalanin sistemski krvni obtok porazdeljuje v tkiva telesa. Zdi se, da D-fenilalanin prečka krvno-možgansko pregrado manj učinkovito kot L-fenilalanin, tako da se majhna količina zaužitega odmerka izloča v urin in v osrednje živčevje ne pride. L-fenilalanin je antagonist za α2δ Ca2+ kanale s Ki of 980 nM.[11] Pri višjih odmerkih ima to lahko vlogo v analgetskih in antidepresivnih lastnostih spojine.
L-fenilalanin deluje kot antagonist za vezavo glicina na NMDA receptor[12] in za vezavo glutamata na AMPA receptor.[13] Na vezavnem mestu glicina na NMDA receptorju ima L-fenilalanin navidezno disociacijsko konstanto KB = 573 µM (ocena po regresiji po Schildu),[14] ki je precej nižja kot je koncentracija L-fenilalanina, ki jo je opaziti pri nezdravljenih primerih fenilketonurije.[15]L-fenilalanin tudi inhibira sproščanje nevrotransmiterjev na glutamatergičnih sinapsah v hipokampusu in korteksu pri koncentracijah , ki jih je videti pri klasični fenilketonuriji, medtem ko ima D-fenilalanin bistveno manjši učinek. [13]
Komercialna sinteza[uredi | uredi kodo]
L-fenilalanin se za medicinske namene, proizvodnjo krme in prehrambenih artiklov, kot je na primer aspartam, v velikih količinah z uporabo bakterije Escherichia coli kot tovarne za aromatske aminokisline kot je fenilalanin. Količine komercialno proizvedenega L-fenilalanina so se povečale s pomočjo genetskega inženiringa, bodisi s spremembami regulativnih promotorjev ali s pomnoženim številom genov za encime, ki so odgovorni za sintezo aminokisline.[16]
Viri[uredi | uredi kodo]
- ↑ Dawson, R. M. C.; in sod. (1959). Data for Biochemical Research. Oxford: Clarendon Press.
- ↑ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature (1983). »Nomenclature and Symbolism for Amino Acids and Peptides«. Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc. Pridobljeno 17. maja 2007.
- ↑ 3,0 3,1 Plimmer, R. H. A. (1912) [1908]. Plimmer, R. H. A.; Hopkins, F. G. (ur.). The Chemical Composition of the Proteins. Monographs on Biochemistry. Zv. Part I. Analysis (2. izd.). London: Longmans, Green and Co. str. 93–97. Pridobljeno 4. junija 2012.
- ↑ Thorpe, T. E. (1913). A Dictionary of Applied Chemistry. Longmans, Green, and Co. str. 191–193. Pridobljeno 4. junija 2012.
- ↑ Harvey M. Ross; June Roth (1. april 1991). The Mood Control Diet: 21 Days to Conquering Depression and Fatigue. Simon & Schuster. str. 59. ISBN 978-0-13-590449-7.
- ↑ http://www.msn.com/en-us/health/medical/15-reasons-why-drinking-diet-soda-and-alcohol-can-kill-you/ss-BBpp9X4#image=13
- ↑ »Aspartame«. UK: Food Standards Agency. Arhivirano iz prvotnega spletišča dne 21. februarja 2012. Pridobljeno 13. marca 2016.
- ↑ Gibbs, R. A.; in sod. (2007). »Evolutionary and Biomedical Insights from the Rhesus Macaque Genome« (pdf). Science. 316 (5822): 222–234. doi:10.1126/science.1139247. PMID 17431167.
- ↑ »D-phenylalanine«. IUPHAR. Arhivirano iz prvotnega spletišča dne 3. marca 2016. Pridobljeno 24. junija 2014.
- ↑ Christianson, D. W.; Mangani, S.; Shoham, G.; Lipscomb, W. N. (1989). »Binding of D-Phenylalanine and D-Tyrosine to Carboxypeptidase A« (pdf). Journal of Biological Chemistry. 264 (22): 12849–12853. PMID 2568989.
- ↑ Mortell KH, Anderson DJ, Lynch JJ, in sod. (Marec 2006). »Structure-activity relationships of alpha-amino acid ligands for the alpha2delta subunit of voltage-gated calcium channels«. Bioorganic & Medicinal Chemistry Letters. 16 (5): 1138–41. doi:10.1016/j.bmcl.2005.11.108. PMID 16380257.
- ↑ Glushakov, AV; Dennis, DM; Morey, TE; Sumners, C; Cucchiara, RF; Seubert, CN; Martynyuk, AE (2002). »Specific inhibition of N-methyl-D-aspartate receptor function in rat hippocampal neurons by L-phenylalanine at concentrations observed during phenylketonuria«. Molecular Psychiatry. 7 (4): 359–67. doi:10.1038/sj.mp.4000976. PMID 11986979.
- ↑ 13,0 13,1 Glushakov, AV; Dennis, DM; Sumners, C; Seubert, CN; Martynyuk, AE (1. april 2003). »L-phenylalanine selectively depresses currents at glutamatergic excitatory synapses«. Journal of neuroscience research. 72 (1): 116–24. doi:10.1002/jnr.10569. PMID 12645085.
- ↑ Glushakov, AV; Glushakova, O; Varshney, M; Bajpai, LK; Sumners, C; Laipis, PJ; Embury, JE; Baker, SP; Otero, DH; Dennis, DM; Seubert, CN; Martynyuk, AE (Februar 2005). »Long-term changes in glutamatergic synaptic transmission in phenylketonuria«. Brain : a journal of neurology. 128 (Pt 2): 300–7. doi:10.1093/brain/awh354. PMID 15634735.
- ↑ Möller, HE; Weglage, J; Bick, U; Wiedermann, D; Feldmann, R; Ullrich, K (december 2003). »Brain imaging and proton magnetic resonance spectroscopy in patients with phenylketonuria«. Pediatrics. 112 (6 Pt 2): 1580–3. PMID 14654669.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Sprenger, G. A. (2007). »Aromatic Amino Acids«. Amino Acid Biosynthesis: Pathways, Regulation and Metabolic Engineering (1. izd.). Springer. str. 106–113. ISBN 978-3-540-48595-7.

