Treonin

| |

| |
| Imena | |
|---|---|
| IUPAC ime
Treonin
| |
| Druga imena
2-amino-3-hidroksibutanojska kislina
| |
| Identifikatorji | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.704 |
| EC število |
|
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Lastnosti | |
| C4H9NO3 | |
| Molska masa | 119,12 g·mol−1 |
| (H2O, g/dl) 10,6 (30 °C), 14,1 (52 °C), 19,0 (61 °C) | |
| Kislost (pKa) | 2,63 (karboksil), 10,43 (amino)[1] |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Treonin (okrajšano kot Thr ali T), je esencialna aminokislina, kar pomeni, da ga človeško telo samo ne more proizvesti, zato ga mora prejemati s hrano. Kodoni, ki zapisujejo treonin, so ACU, ACC, ACA in ACG.
Oblike
[uredi | uredi kodo]Zaradi alkoholne stranske verige sodi med polarne aminokisline. Poleg izolevcina je ena od dveh aminokislin, ki imata tudi v stranski verigi kiralni center, zato so možni štirje stereoizomeri, vključno z dvema diastereoizomeroma L-treonina.
  |
| L-treonin (2S,3R) in D-treonin (2R,3S) |
 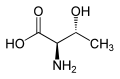 |
| L-alo-treonin (2S,3S) in D-alo-treonin (2R,3R) |
Zgodovina
[uredi | uredi kodo]Treonin je bila zadnja odkrita proteinogena aminokislina, prvi jo je opisal William Cumming Rose leta 1935. Spojina je bila poimenovana zaradi podobnosti s treozo, monosaharidom iz štirih ogljikovih atomov.[2]
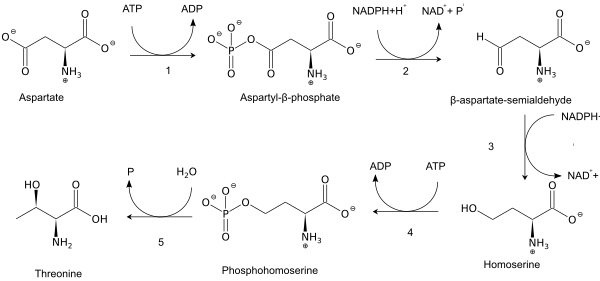
Biosinteza
[uredi | uredi kodo]Je esencialna aminokislina, torej je živalski organizmi ne sintetizirajo in jo morajo pridobiti s hrano, predvsem v obliki beljakovin. V rastlinah in mikroorganizmih se treonin sintetizira v več korakih iz asparaginske kisline preko homoserina.
Metabolizem
[uredi | uredi kodo]Razgradnja poteka po dveh poteh:
- Preko piruvata z encimom treonin dehidrogenazo, intermediati te poti se vključujejo v sintezo acetil-CoA in glicina.
- Po manj običajni poti pri človeku preko ketobutirata do sukcinil-CoA.
Viri
[uredi | uredi kodo]- ↑ Dawson, R.M.C., et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ↑ Meyer, Curtis (20. julij 1936). »The Spatial Configuation of Alpha-Amino-Beta-Hydroxy-n-Butyric Acid« (PDF). Journal of Biological Chemistry. 115 (3).