Prolin

| |

| |
| Imena | |
|---|---|
| IUPAC ime
prolin
| |
| Sistematično ime
pirolidin-2-karboksilna kislina[1] | |
| Identifikatorji | |
3D model (JSmol)
|
|
| 80812 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.009.264 |
| EC število |
|
| Gmelin | 26927 |
| KEGG | |
| MeSH | Proline |
PubChem CID
|
|
| RTECS število |
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Lastnosti | |
| C5H9NO2 | |
| Molska masa | 115,13 g·mol−1 |
| Videz | Prozorni kristali |
| Tališče | 205–228 °C (401–442 °F; 478–501 K) (razpada) |
| Topnost | 1.5g/100g ethanol 19 degC[2] |
| log P | -0.06 |
| Kislost (pKa) | 1.99 (carboxyl), 10.96 (amino)[3] |
| Nevarnosti | |
| S-stavki (zastarelo) | S22, Predloga:S24/25 |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Prolin (skrajšano Pro ali P; kodirajo ga s kodoni CCU, CCC, CCA, in CCG) je α-amino kislina, ki se uporablja v biosintezi proteinov. Vsebuje α-amino skupino (ki je v bioloških pogojih v protonirani >NH2+ obliki,), α-karboksilno kislinsko skupino (v bioloških pogojih v deprotonirani −COO− obliki), in kot stransko verigo pirolidin, kar prolin razvršča med nepolarne (pri fiziološkem pH), alifatske amino kisline. Prolin za ljudi ni bistvena amino kislina, naše telo ga lahko sintetizira iz ne-esencialne amino kisline L-glutamata.
Prolin je edina amino kislina, ki vsebuje dodaten amin. Poleg tega je prolin edinstven tudi zato, ker je alfa-amino skupina pritrjena neposredno na stransko verigo, tako da kar α ogljik sam neposredno substituira stransko verigo.
Zgodovina in etimologija
[uredi | uredi kodo]Prolin je prvič izoliral leta 1900 Richard Willstätter, ki je amino kislino sintentiziral med preučevanjem N-metilprolina. Leto kasneje je Emil Fischer objavil metodo, s katero se prolin sintetizira iz ftalimid propilmalonskega estra.[4] Ime prolin izvira iz pirolidina, enega od gradnikov spojine.[5]
Bio sinteza
[uredi | uredi kodo]Prolin v biosintezi nastaja iz amino kisline L-glutamata. Glutamat-5-semialdehid se najprej tvori z (ATP-odvisno) glutamat 5-kinazo in glutamat-5-semialdehid dehidrogenazo (ki potrebuje NADH ali NADPH). Peri tem lahko pride spontano do nastanka obroča in 1-pirolin-5-karboksilne kisline, ki jo pirolin-5-bromopiridin karboksilat reduktaza (ob uporabi NADH ali NADPH) reducira, ali pa jo ornitin aminotransferaza pretvori v ornitin, ki ga nato ornitin ciklodeaminaza pretvori v prolin.[6]

Biološka aktivnost
[uredi | uredi kodo]Za L-Prolin so ugotovili, da deluje kot šibek agonist za receptor glicina in za NMDA ter ne-NMDA (AMPA/kainat) ionotropska receptorja za glutamat.[7][8][9] Obstaja hipoteza, da gre za možen endogen ekscitotoksin.[7][8][9] V rastlinah je akumulacija prolina običajen fiziološki odgovor na različne strese, poleg tega pa tudi del razvojnega programa v rodnih tkivih (kot je npr. cvetni prah).[10]
Proline je marker za fosforilacijo in ga pogosto najdemo tik pred aminokislinama serinom in treoninom, označuje ju kot možni mesti za fosforilacijo. Mesto prolina pred tema amino kislinama v aminokislinski verigi je z razvojnega vidika visoko ohranjeno.
Lastnosti v strukturi beljakovin
[uredi | uredi kodo]Značilna ciklična struktura prolinove stranske verige mu daje v primerjavi z drugimi aminokislinami izjemno konformacijsko togost. To vpliva tudi na stopnjo nastanka peptidnih vezi med prolinom in drugimi aminokislinami. Če se prolin v peptidno vez veže kot amid, njegov dušik ni vezan na kak vodik, kar pomeni, da ne more delovati kot darovalec vodikovih vezi darovalca, lahko pa vodikovo vez sprejema.
Nastanek peptidne vezi z vhodno Pro-tRNAPro je precej počasnejši kot pa pri kateri katerokoli drugi tRNA, kar je na splošno značilno za N-alkilamino kisline.[11] Nastanek peptidni vezi je počasen tudi, kadar gre za vhodno tRNA in verigo, ki se končuje v prolinu; nastanek vezi prolin-prolin traja dlje kot vse druge možnosti.[12]
Izjemna konformacijska togost prolina vpliva na sekundarno strukturo proteinov v okolici prolinskih residuov in je lahko vzrok za večjo pogostnost aminokisline v beljakovinah termofilnih organizmov. Sekundarno strukturo beljakovin je mogoče opisati z dihedralnimi koti φ, ψ in ω v beljakovinski hrbtenici. Ciklična struktura prolinove stranske verige priklene kot φ na približno -65°.[13]
Prolin deluje kot strukturni disruptor med rednimi elementi drugotne strukture, kot so alfa vijačnice in beta listi; vendar pa je prolin najti običajno kot prvi residuum alfa vijačnice, pa tudi na robu beta listov. Prolin tudi pogosto najdemo v ovinkih (dodatni obliki drugotne strukture), kjer je v pomoč pri nastanku beta ovinkov. To je lahko vzrok za zanimivo dejstvo, da je prolin običajno izpostavljen topilom, čeprav ima popolnoma alifatsko stransko verigo.
Zaporedje prolinov in/ali hidroksiprolinov lahko tvori poliprolinsko vijačnico, ki prevladuje v drugotni strukturi kolagena. Hidroksilacija prolina (bodisi s prolil hidroksilazo, bodisi z drugimi dodatki, ki odjemljajo elektron, kot je recimo fluor) bistveno poveča konformacijsko obstojnost kolagena.[14] Hidroksilacija prolina je zato kritičen biokemijski proces, ki skrbi za ohranjanje vezivnega tkiva višjih organizmov. Zaradi napak pri tej hidroksilaciji lahko pride do resnih bolezni, na primer do skorbuta; vzrok zanje je lahko v mutaciji v encimu prolil hidroksilaza ali pomanjkanje askorbata (vitamina C) kot nujnega kofaktorja.
Cis-trans izomerizacija
[uredi | uredi kodo]Peptidni vezi s prolinom in drugimi N-substituiranimi amino kislinami (kot recimo sarkozin), obstajajo lahko tako s cis kot tudi trans izomeri. Večina peptidnih vezi se odloči za trans izomer (običajno 99.9 % pod neobremenjenimi pogoji), predvsem zato, ker amidov vodik (trans izomer) predhodni Cα atom odbija manj kot pa naslednji Cα atom (cis izomer). Drugače pri peptidni vezi X-Pro (kjer X predstavlja katerikoli amino kislino), kjer sta tako cis kot trans izomer vezi v prostorskem konfliktu s sosedom in s stališča energije skoraj enakovredna. Zato znaša pod neobremenjenimi pogoji delež peptidne vezi X-Pro v obliki cis izomera 10-40 %; pri čemer je nekoliko odvisen od predhodne amino kisline - aromatičnim residuom je cis izomer nekoliko bolj pri srcu.
Iz kinetičnega vidika je cis-trans izomerizacija prolina zelo počasen proces. Ovira lahko zlaganje beljakovine, če se en ali več za zlaganje ključnih prolinskih ostankov znajdejo v ne-nativni izomerni obliki, še posebej, kadar nativna beljakovina zahteva cis izomer. Vzrok za to je sinteza v v ribosomih, kjer se prolin v verigo dodaja izključno samo kot trans izomer. Vsi organizmi imajo na voljo prolil izomerazo, encim, ki to izomerizacijo katalizira; nekatere bakterije tudi poznajo specializirane prolil izomeraze, ki se povezujejo z ribosomi. Za zlaganje beljakovine pa prolini v njej niso nujno vsi bistvenega pomena; proces zlaganja lahko poteka z običajno hitrostjo, tudi kadar se številne peptidne vezi X-Pro nahajajo v obliki, ki ni nativna.
Uporaba
[uredi | uredi kodo]Proline in njegovi derivati se pogosto uporabljajo kot asimetrični katalizatorji v organokatalitičnih reakcijah. Redukcija CBS in aldol kondenzacija, ki jo katalizira prolin, sta za to tipična primera.
L-Prolin ščiti pred osmozo in se zato uporablja v številnih farmacevtskih in biotehnoloških postopkih. Pri varjenju piva se na prolinu bogate beljakovine vežejo s polifenoli, kar povzroča motnost tekočine. [15]
Posebnosti
[uredi | uredi kodo]Prolin in glicin sta aminokislini , ki ne ustrezata tipičnemu Ramachandranovemu diagramu. Zaradi nastanka obroča, vezanega na beta ogljik, imata kota ψ in φ okoli peptidne vezi omejeno možnost rotacije. Prolin je zato pogosto najti na "ovinkih" v beljakovini, ker njegova prosta entropija (ΔS) v primerjavi z veliko drugimi aminokislinami ni velika, kar pomeni, da je sprememba entropije med zloženo in nezloženo obliko manjša. Prolin tako le redko najdemo v strukturah α in β, njegova prisotnost bi zmanjšala stabilnost teh struktur, saj njegova stranska veriga α-N lahko tvori samo eno vodikovo vez.
Poleg tega je prolin edina amino kislina, ki po uporabi ninhidrina v kromatografiji ne razvije modre/vijolične barve, temveč se obarva oranžno/rumeno.
Zgodovina
[uredi | uredi kodo]Richard Willstätter je prolin sintetiziral leta 1900 v reakciji natrijeve soli dietil malonata z 1,3-dibromopropanom. Leta 1901 je Hermann Emil Fischer izolirasl prolin iz kazeina in razpadnih produktov γ-ftalimido-propilmalonskega estra.[16]
Glej tudi
[uredi | uredi kodo]Sinteza
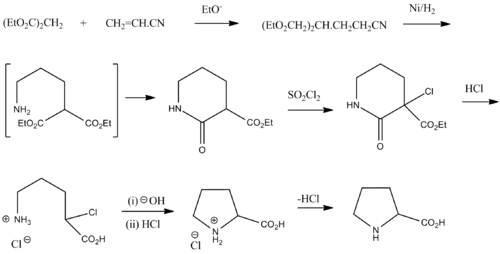
[uredi | uredi kodo]Racemični prolin je mogoče sintetizirati iz dietil malonata in akrilonitrila:[17]
Sklici
[uredi | uredi kodo]- ↑ http://pubchem.ncbi.nlm.nih.gov/summary/summary.cgi?cid=614&loc=ec_rcs
- ↑ H.-D. Belitz; W. Grosch; P. Schieberle. Food Chemistry. str. 15. ISBN 978-3-540-69933-0.
- ↑ Nelson, D.L., Cox, M.M., Principles of Biochemistry. NY: W.H. Freeman and Company.
- ↑ »Proline«.
- ↑ »proline«. American Heritage Dictionary of the English Language, 4th edition. Pridobljeno 6. decembra 2015.
- ↑ Lehninger, Albert L.; Nelson, David L.; Cox, Michael M. (2000), Principles of Biochemistry (3rd izd.), New York: W. H. Freeman, ISBN 1-57259-153-6
- ↑ 7,0 7,1 Ion Channel Factsbook: Extracellular Ligand-Gated Channels. Academic Press. 16. november 1995. str. 126–. ISBN 978-0-08-053519-7.
- ↑ 8,0 8,1 Henzi V; Reichling DB; Helm SW; MacDermott AB (1992). »L-proline activates glutamate and glycine receptors in cultured rat dorsal horn neurons«. Mol. Pharmacol. Zv. 41, št. 4. str. 793–801. PMID 1349155.[mrtva povezava]
- ↑ 9,0 9,1 Orhan E. Arslan (7. avgust 2014). Neuroanatomical Basis of Clinical Neurology, Second Edition. CRC Press. str. 309–. ISBN 978-1-4398-4833-3.
- ↑ Verbruggen N; Hermans C (2008). »Proline accumulation in plants: a review«. Amino Acids. Zv. 35, št. 4. str. 753–759. doi:10.1007/s00726-008-0061-6. PMID 18379856.
- ↑ Pavlov, Michael Y; Watts, Richard E; Tan, Zhongping; Cornish, Virginia W; Ehrenberg, Måns; Forster, Anthony C (2010), »Slow peptide bond formation by proline and other N-alkylamino acids in translation«, PNAS, 106 (1): 50–54, doi:10.1073/pnas.0809211106, PMC 2629218, PMID 19104062.
- ↑ Buskirk, Allen R.; Green, Rachel (2013). »Getting Past Polyproline Pauses«. Science. Zv. 339, št. 6115. str. 38–39. doi:10.1126/science.1233338.
- ↑ Morris, Anne (1992). »Stereochemical quality of protein structure coordinates«. Proteins: Structure, Function, and Bioinformatics. Zv. 12. str. 345–364. doi:10.1002/prot.340120407. PMID 1579569.
{{navedi revijo}}:|access-date=potrebuje|url=(pomoč) - ↑ Szpak, Paul (2011). »Fish bone chemistry and ultrastructure: implications for taphonomy and stable isotope analysis«. Journal of Archaeological Science. Zv. 38, št. 12. str. 3358–3372. doi:10.1016/j.jas.2011.07.022.
- ↑ K.J. Siebert, "Haze and Foam",[1] Accessed July 12, 2010.
- ↑ R.H.A. Plimmer (1912) [1908], R.H.A. Plimmer & F.G. Hopkins (ur.), The chemical composition of the proteins, Monographs on biochemistry, zv. Part I. Analysis (2. izd.), London: Longmans, Green and Co., str. 130, pridobljeno 20. septembra 2010
- ↑ Vogel, Practical Organic Chemistry 5th edition
Nadaljnje branje
[uredi | uredi kodo]- Balbach, J.; Schmid, F. X. (2000), »Izomerizacija prolina in kataliza pri zlaganju beljakovin«, v Pain, R. H. (ur.), Mehanizmi zlaganja beljnakovin (2. izd.), Oxford University Press, str. 212–49, ISBN 0-19-963788-1), Oxford University Press, pp. 212–49, ISBN 0-19-963788-1 .
- Za poglobljen znanstven pregled motenj pri presnovi prolina in hidroksiprolina glej pogl. 81 v OMMBID Charles Scriver, Beaudet, A.L., Valle, D., Sly, W.S., Vogelstein, B., Childs, B., Kinzler, K.W. (Accessed 2007). The Online Metabolic and Molecular Bases of Inherited Disease. New York: McGraw-Hill. - Glej tudi OMMBID blog Arhivirano 2007-02-06 na Wayback Machine..