Karboksilna kislina
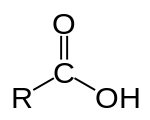

Karboksílne kislíne so organske spojine, ki vsebujejo eno ali več karboksilnih skupin −C(=O)OH, ki se običajno pišejo kot −COOH.[1] So donorji protonov (oddajajo vodikov H+ ion) in potemtakem sodijo med Brønsted-Lowryjeve kisline. Soli in anione karboksilnih kislin imenujemo karboksilati.
Najenostavnejše predstavnice karboksilnih kislin so alkanojske kisline s splošno formulo R−COOH, v kateri je R vodik ali alkilni radikal.
Fizikalne lastnosti[uredi | uredi kodo]

Karboksilne kisline so polarne spojine in tvorijo vodikove vezi. Pri visokih temperaturah izparijo. V plinski fazi se običajno nahajajo v dimerni obliki. Nižje karboksilne kisline z 1–5 ogljikovi atomi so zaradi velike polarnosti topne v vodi, z naraščanjem števila ogljikovih atomov pa njihova polarnost pada in postajajo vedno bolj hidrofobne. Višje kisline se zato bolje topijo v manj polarnih topilih, na primer v etrih in alkoholih.[2]
Karboksilne kisline so šibke kisline, se pravi da v vodni raztopini le delno disociirajo na karboksilne in vodikove ione: RCOOH ⇌ RCOO− + H+
Pri sobni temperaturi v vodni raztopini disociira samo 0,02 % ocetne kisline.
Stabilnost kisline[uredi | uredi kodo]
Kislost karboksilnih kislin se lahko pojasni ali s stabilnostjo kisline ali s stabilnostjo konjugirane baze, za razlago pa se lahko uporabi ali induktivne ali resonančne pojave v −COOH skupini.
Če se za razlago kislosti uporabi induktivne pojave, se kislost lahko razloži z dvema elektronegativnima kisikovima atomoma, ki odbijata elektronski oblak okoli vezi O−H in jo s tem oslabita. Šibka vez O−H zmanjša stabilnost molekule kisline. Vodikov atom je zato bolj stabilen in zlahka disociira v H+ ione. Ker je kislina nestabilna, je ravnotežje reakcije pomaknjeno v desno.
Dodatni elektronegativni atomi ali atomske skupine, ki so vezani na kislino, na primer −Cl ali −OH, imajo podoben, vendar manjši vpliv. Prisotnost teh skupin poveča kislost zaradi induktivnega učinka. Primer: trikloroocetna kislina, ki ima tri −Cl atome, je močnejša od mlečne kisline, ki ima eno –OH skupino, ta pa je močnejša od ocetne kisline, ki nima vezane nobene elektronegativne substituente.
Stabilnost konjugirane baze[uredi | uredi kodo]

Kislost karboksilnih kislin se lahko pojasni tudi z resonančnimi pojavi.
Z disociacijo karboksilne kisline nastane resonančno stabiliziran produkt, katerega negativni naboj je razdeljen oziroma delokaliziran med dva kisikova atoma. Vsaka vez C−O ima zato značilnosti tako imenovane delne dvojne vezi. Ker je konjugirana baza stabilna, je ravnotežje reakcije pomaknjeno v desno.
Spektroskopija[uredi | uredi kodo]
Karboksilne kisline je najlaže identificirati z infrardečo spektroskopijo. Pri valovnih dolžinah od 1680 do 1725 cm-1 je prepoznavno raztezanje vezi C=O, pri 2500 do 3000 cm-1 pa raztezanje vezi O-H v karboksilni skupini.[2]
V spektroskopiji 1H JMR se na področju 10–13 μm prikaže vodik iz hidroksilne skupine. Vodik je pogosto nejasen ali celo neopazen in se zlahka zamenja s sledovi vode.
Nahajališča[uredi | uredi kodo]
Karboksilne kisline, njihove soli in estri so zelo razširjeni naravni produkti.
Nižje alifatske karboksilne kisline z ravnimi verigami, pa tudi tiste z do 18 ogljikovimi atomi, se proizvajajo tudi industrijsko. Ocetna kislina, na primer, se proizvaja iz metanola in ogljikovega monoksida, kisline z velikim številom ogljikovih atomov pa s hidrolizo trigliceridov iz rastlinskih in živalskih maščob.
Ocetna kislina se proizvaja tudi s fermentacijo etanola in se kot kis uporablja izključno v prehrambeni industriji.
Sinteze[uredi | uredi kodo]
Industrijske sinteze[uredi | uredi kodo]
- Z oksidacijo primarnih alkoholov in aldehidov z močnimi oksidanti, na primer h kalijevim dikromatom (K2Cr2O7), kromovo kislino (CrO3 + H2So4), kalijevim permanganatom (KMnO4) ali natrijevim kloritom (NaClO2).
- Z oksidativnim cepljenjem olefinov z ozonolizo, kalijevim permanganatom ali kalijevim dikromatom. V karboksilne kisine se oksidirajo tudi vse alkilne skupine na benzenovem obroču, ne glede na dolžino verige. Na ta način se industrijsko pridobiva benzojeva kislina iz toluena.
- S hidrolizo nitrilov, estrov in amidov v kislem ali bazičnem mediju.
- Z delovanjem Grignardovega reagenta na ogljikov dioksid. Sinteza se v industriji ne uporablja.
Druge sinteze[uredi | uredi kodo]
Karboksilne kisline se lahko sinetizirajo tudi z naslednjimi reakcijami:
- Z disproporcionacijo aldehidov v Canizzarovi reakciji.
- S prerazporeditvijo diketonov.
- S halogeniranjem in kasnejšo hidrolizo metil ketonov.
- S hidroformiliranjem in kasnejšo hidrolizo alkenov (Kochova reakcija).
- Manj pogoste so sinteze benzojskih kislin iz nitrobenzenov z von Richterjevo reakcijo in fenolov s Kolbe-Schmittovo reakcijo.
Reakcije[uredi | uredi kodo]
- Karboksilne kisline tvorijo z bazami soli – karboksilate, v katerih je vodik iz hidroksilne skupine (−OH) v karboksilni skupini (−COOH) zamenjan s kovinskim kationom. Primer: ocetna kislina reagira z natrijevim bikarbonatom, pri čemer nastanejo natrijev acetat, ogljikov dioksid in voda:
- CH3COOH + NaCO3H → CH3COONa + CO2 + H2O
- CH3COOH + C2H5OH → CH3COOC2H5 + H2O
- CH3COOH + C2H5NH2 → C3CONHC2H5 + H2O
- Hidroksilna skupina v karboksilni skupini se obnaša podobno kot v alkoholih in fenolih in se v reakciji s tionil kloridom (SOCl2) substituira s klorom, pri čemer nastanejo acil kloridi:
- R−COOH + SOCl2 → R−COCl + SO2 + HCl
- Karboksilna skupina ima zaradi keto-enolne tavtomerije na α-ogljikovem atomu nestabilen proton (H+), ki se zlahka substituira s halogenom (halogeniranje Hell-Volhard-Zelinsky):
- Arndt-Eistertova sinteza vrine na karboksilno kislino α–metilensko skupino in podaljša ogljikovo verigo za en C atom:
- Curtiusova prerazporeditev pretvori karboksilne kisline v izocianate:
- Schmidtova reakcija pretvori karboksilne kisline v amine:
- Hunsdieckerjeva reakcija pretvori karboksilne kisline v alifatske halogenide:
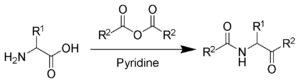
- Dakin-Westova reakcija pretvori aminokisline v ustrezne amino ketone:
- Barbier-Wielandova degradacija: α–metilenska skupina (−CH2−) v alifatskih karboksilnih kislinah se v nizu stopenjskih reakcij odcepi, tako da se veriga ogljikovih atomov skrajša.[3][4]
- Adicija karboksilne skupine na neko spojino se imenuje karboksiliranje, eliminacija karboksilne skupine pa dekarboksiliranje. Tovrstne reakcije katalizirajo encimi karboksilaze (EC 6.4.1) in dekarbokslaze (EC 4.1.1.).
Nomenklatura in primeri[uredi | uredi kodo]
Karboksilne kisline poimenujemo s pripono -ojska (npr. heksanojska kislina). Številne karboksilne kisline, zlasti tiste bolj znane, imajo tudi starejša trivialna imena, ki ne sledijo pravilom nomenklature; nekatera med njimi so se zelo uveljavila in se uporabljajo pogosteje kot IUPAC-imena (mravljična, ocetna, maslena kislina ...).
| Št. C-atomov | Splošno ime | IUPAC-ime | Kemijska formula | opis |
|---|---|---|---|---|
| 1 | mravljinčna kislina | metanojska kislina | HCOOH | pik žuželk, tekočina v zadku mravelj |
| 2 | ocetna kislina | etanojska kislina | CH3COOH | v kisu |
| 3 | propionska kislina | propanojska kislina | CH3CH2COOH | |
| 4 | maslena kislina | butanojska kislina | CH3(CH2)2COOH | žaltavo maslo |
| 5 | valerijanska kislina | pentanojska kislina | CH3(CH2)3COOH | v baldrijanu |
| 6 | kapronska kislina | heksanojska kislina | CH3(CH2)4COOH | |
| 7 | enantična kislina | heptanojska kislina | CH3(CH2)5COOH | |
| 8 | kaprilna kislina | oktanojska kislina | CH3(CH2)6COOH | kokosovo in materino mleko |
| 9 | pelargonjska kislina | nonanojska kislina | CH3(CH2)7COOH | |
| 10 | kaprinska kislina | dekanojska kislina | CH3(CH2)8COOH | |
| 12 | lavrinska kislina | dodekanojska kislina | CH3(CH2)10COOH | kokosovo olje |
| 16 | palmitinska kislina | heksadekanojska | CH3(CH2)14COOH | |
| 18 | stearinska kislina | oktadekanojska | CH3(CH2)16COOH | voski, mila |
| mlečna kislina | 2-hidroksipropanojska kislina | CH3CH(OH)COOH | kislo mleko, kislo zelje |
Glavne skupine karboksilnih kislin so:
- nenasičene monokarboksilne kisline s kratkimi verigami: akrilna kislina (2-propenojska kislina, CH2=CH−COOOH), ki je surovina za sintezo poliakrilatov
- nasičene in nenasičene maščobne kisline s srednje dolgimi in dolgimi verigami s sodim številom ogljikovih atomov: palmitinska, stearinska, oleinska kislina...
- aminokisline – gradniki beljakovin: valin, fenilalanin ...
- ketokisline – biološko pomembne karboksilne kisline s keto skupino: piruvična, acetocetna kislina...
- aromatske karboksilne kisline: benzojska, salicilna kislina ...
- dikarboksilne kisline, ki vsebujejo dve karboksilni skupini: oksalna, malonska, jantarna...
- trikarboksilne kisline, ki vsebujejo tri karboksilne skupine: citronska, akonitinska kislina...
- α-hidroksikarboksilne kisline, ki imajo na ogljikovem atomu ob karboksilni skupini vezano hidroksilno skupino: mlečna kislina...
Reference[uredi | uredi kodo]
- ↑ Compendium of Chemical Terminology, carboxylic acids, accessed 15 Jan 2007.
- ↑ 2,0 2,1 R.T. Morrison, R.N. Boyd. Organic Chemistry, 6th Ed. (1992) ISBN 0-13-643669-2.
- ↑ Organic Syntheses, Coll. Vol. 3, p.234 (1955); Vol. 24, p.38 (1944) Link
- ↑ Organic Syntheses, Coll. Vol. 3, p.237 (1955); Vol. 24, p.41 (1944) Link.