Korozija

Korozíja je razdiralni napad na kovino in najpogosteje temelji na elektrokemijskih reakcijah, ki potekajo zaradi termodinamske nestabilnosti materiala v nekem okolju. Je kompleksen proces, ki je odvisen od mnogih dejavnikov, predvsem od metalurških značilnosti kovine oziroma zlitine (kemična sestava, mikrostruktura, vključki, faza snovi), lastnosti korozijskega medija (prevodnost, temperatura, pH) in prisotnosti različnih površinskih filmov, ki lahko ščitijo kovino.
Kovina, ki korodira, je pravzaprav kratkostično zvezan galvanski člen, ki obsega tri primarne elektrokemijske procese: anodno reakcijo, transport elektronov po kovini in ionov po elektrolitu, ter katodno reakcijo. Kovine oziroma njihove zlitine so vedno nekoliko heterogene, že zaradi različne orientacije kristalnih zrn in nepravilnosti v kristalni mreži. V večini primerov vsebujejo posamezne vključke in različne faze, ki se med seboj razlikujejo glede na njihov elektrodni potencial. Zato v raztopini elektrolitov posamezna mesta delujejo kot anoda, preostale površine pa kot katoda. Korozijske poškodbe povzroča anodna reakcija (oksidacija), pri kateri se iz kovine v elektrolit odtapljajo pozitivno nabiti kovinski ioni v kovini pa ostajajo elektroni. Elektroni po kovini potujejo do mesta katodne reakcije (redukcija), kjer se vežejo s kationi (npr. H+) ali nevtralnimi molekulami v raztopini (npr. O2). Procesa oksidacije in redukcije sta vedno uravnotežena: kolikor elektronov se sprosti pri anodni reakciji, toliko se jih porabi pri katodni reakciji. Korozijska reakcija se ustavi, ko preneha delovati katodna oziroma anodna reakcija.
Kemija korozije[uredi | uredi kodo]
Z nekaj izjemami so čiste kovine v zemeljski atmosferi termodinamsko nestabilne, kar pomeni, da spontano reagirajo z okolico in prehajajo v stabilnejše spojine. V naravi se večina kovin nahaja v obliki oksidov in sulfidov, ki jih je z veliko vložene energije mogoče pretvoriti nazaj do čistih kovin.

Čeprav je ena izmed lastnosti poliranih kovin tudi visok sijaj, kar daje občutek homogenosti materiala, je mikroskopska slika kovinske površine precej drugačna. Pri običajnih metalurških postopkih pridobivanja kovin iz rude nastanejo mikrokristalinične strukture, kar povzroči razlike v kemijskih lastnostih materiala na mikroskopski ravni. Po celotni površini kovine tako ne poteka enotna reakcija, pač pa več različnih. Poleg razlik v stukturi na različne kemijske lastnosti materiala vplivajo tudi drugi dejavniki, kot na primer prisotnost oksidov, adsorbiranih molekul ter razlike v lokalni koncentraciji elektrolita.

Ko površina kovine pride v stik z elektrolitom, zaradi razlik v kemijskih lastnostih posameznih področij kovine nastanejo mikrogalvanski členi, ki začnejo korozijo. V sistemu so prisotna katodna in anodna področja, med katerimi je vzpostavljen električni kontakt, po katerem se gibljejo elektroni, medtem ko elektrolit služi kot medij za prenos ionov. Elektrolit po navadi predstavlja večjo množino snovi, ki obliva material, ali pa se pojavi kot tanka kondenzirana plast na površini. V običajnem okolju največji delež elektrolitov zavzemajo vodne raztopine. Te po navadi vsebujejo različne koncentracije organskih in anorganskih ionov ter molekul. Ko je elektrolit v stiku z zrakom, se raztopina nasiti tudi s kisikom in ogljikovim dioksidom, ki pogosto sodelujeta pri procesu korozije.
Reakcije, ki potekajo pri korozijskih procesih, so večinoma elektrokemijske; med reaktanti pride do prenosa elektrona, kar privede do spremembe oksidacijskega števila atomov. Razdelimo jih v dve skupini:
- Anodne reakcije, kjer običajno poteka oksidacija kovin:
- Katodne reakcije, kjer poteka redukcija ionskih zvrsti. V kislih vodnih raztopinah poteka redukcija H+ ionov:
Če je v raztopini elektrolita raztopljen tudi kisik, pogosto potekajo tudi naslednje reakcije:
Celotna reakcija, ki poteka med procesom korozije, je sestavljena iz anodne reakcije in mešanice katodnih reakcij, kar skupaj tvori galvanski člen. Na anodi poteka oksidacija, med katero pride do odtapljanja kovine in nastajanja kovinskih ionov, medtem pa na katodi lahko poteka več različnih reakcij naenkrat. Pri reakcijah nastajajo topni (M+) in netopni (oksidi, nekateri hidroksidi) ter plinasti (H2) korozijski produkti. Tekom korozije se poleg materiala pogosto spremeni tudi sestava elektrolita, kar vpliva na položaj ravnotežja in hitrosti posameznih kemijskih reakcij.
Sistem postane kompleksnejši z dodajanjem novih komponent. Prisotnost drugih kovinskih ionov v raztopini omogoči dve novi katodni reakciji: znižanje oksidacijsega stanja kovinskega iona ter elektrodepozicijo kovine na material:
Na položaj ravnotežja vplivajo tudi različni ligandi, ki s kovinami tvorijo tako topne kot tudi netopne komplekse:
Pod določenimi pogoji v raztopinah pride do redukcije oksidirajočih kislin:
Slednja reakcija je celo zaželena, saj zaustavlja proces korozije.
Svojevrsten problem predstavljajo sistemi kontaminirani z mikroorganizmi. Ti s svojimi presnovnimi produkti v sistem lahko vnesejo nove korozivne zvrsti. Bakterije vrste desulphovibrio desulphurican[1][2] so na primer sposobne reducirati sulfate v zelo nevarne sulfide:
Ti nadalje reagirajo in tvorijo nove korozijske produkte:
Gornji pregled reakcij ni popoln, vendar pokaže kompleksnost korozijskih procesov. Realni korozijski sistemi so zelo dinamični, saj se količine reaktantov neprestano spreminjajo, od česar je odvisen tudi nabor in potek kemijskih reakcij v sistemu.
Termodinamika korozije[uredi | uredi kodo]
V nasprotju z galvanskimi členi in gorivnimi celicami, kjer za normalno delovanje sistema potrebujemo dve elektrodi, anodo in katodo, je v korozijskih sistemih dovolj ena sama elektroda. Sistem se imenuje enoelektrodni sistem, elektroda pa simultano opravlja vlogo elektronskega izvira in ponora. Fenomen se pojavi zaradi lokalnih razlik v kemijski strukturi materaiala in deluje na podoben način kot običajni galvanski člen.
Termodinamsko zvezo v korozijskih sistemih je mogoče opisati z Nernstovo enačbo[3]:
Standardne napetosti za posamezne elektrodne reakcije so razvrščene v elektrokemijsko vrsto, iz katere je na primer mogoče razbrati, katere kovine so korozijsko odpornejše od drugih.
V praksi se pogosto izkaže, da so korozijski sistemi preveč zapleteni, da bi bilo mogoče z uporabo Nernstove enačbe natančno napovedati termodinamsko obnašanje sistema. V ta namen se je namesto elektrokemijske vrste razvila t. i. galvanska vrsta. Ta je nastala z eksperimentalnim opazovanjem kovin v določenem okolju z upoštevanjem vseh dejavnikov in prikazuje realtivno odpornost sistema na korozijo.

Kljub vsemu je Nernstova enačba dovolj univerzalna za oceno termodinamske stabilnosti sistema. Ob upoštevamo, da je v korozijskem sistemu ena izmed možnih reakcij tudi redukcija protonov v vodik, je mogoče Nernstovo enačbo zapisati kot:
oziroma:
Diagram, ki prikazuje odvisnost reverzibilne napetosti elektrode od pH se imenuje Paurbaixov diagram. Iz diagrama je mogoče izluščiti informacije o termodinamski stabilnosti posameznih faz in oceniti termodinamski potek korozije. Konstrukcija Paurbaixovih diagramov še vedno ne upošteva kinetičnih dejavnikov, ki nastopajo pri koroziji, zato je pri interpretaciji potrebna pazljivost. Iz Paurbaixovih diagramov je razvidno da večina kovin ni termodinamsko stabilnih. Pogosto je korozija precej počasen proces, kar pomeni, da so reakcije tudi kinetično kontrolirane.
Kinetika korozije[uredi | uredi kodo]
Pri potopitvi kovine v elektrolit pride na fazni meji do ločevanja nabojev, pri čemer se vzpostavi električna dvoplast debeline nekaj nanometrov. Prenos elektronov, ki poteka med kemijsko reakcijo ni več neoviran, saj se elektroni gibljejo v močnem električnem polju. Ko je hitrost kemijske reakcije pogojena izključno s prenosom elektronov med elektrodo in posamezno zvrstjo, kinetiko korozijskega sistema opisuje Butler-Volmerjeva enačba:[4]
ki predstavlja odvisnost gostote korozijskega toka od prenapetosti v sistemu. Natančen potek kemijskih reakcij pri koroziji pogosto ni znan, vendar lahko v Butler-Volmerjevo enačbo uvedemo eksperimetalne koeficiente in izmerimo Taflovo krivuljo:
Butler-Volmerjeva enačba opisuje zvezo med gostoto toka in potencialom elektrode z uporabo treh enostavno določljivih spremenljivk; in .
Določanje Taflovih krivulj je osnovnejša, vendar zelo učinkovita metoda za določanje kinetičnih parametrov izbranega korozijskega sistema. Rezultat meritve je krivulja, ki predstavlja odvisnost napetosti od logaritma toka. Spremenljivke, ki nastopajo v Butler-Volmerjevi enačbi, je mogoče določiti iz linearnih delov katodnega, oziroma anodnega področja. Poleg tega je iz oblik krivulje mogoče oceniti tudi hitrost korozije ter način pasivacije. Taflova krivulja ni primerna za določanje tipa korozije v izbranem sistemu, zato je potrebno uporabiti kompleksnejše metode.
Tipi korozije[uredi | uredi kodo]
Kemijska in konstrukcijska raznolikost uporabnih sistemov nam poleg termodinamske in kinetične pestrosti ponuja tudi izbor različnih tipov korozije. Precej malo verjetno je, da bi na vseh sistemih korozija potekala na enak način. Posamezen tip korozije je najenostavneje določiti z opazovanjem, če pa dovolj dobro poznamo sestavo sistema, lahko način korozije do neke mere napovemo v naprej, saj se isti tip korozije po navadi ponavlja ob določenem vzorcu korozijskih dejavnikov.


Enakomerna korozija[uredi | uredi kodo]
Enakomerna korozija je najpogostejša oblika korozije. Sistem korodira po celotni površini oziroma po večjem delu površine, ki je izpostavljena korozivnemu mediju. Povzroča tanjšanje materiala, kar v končni fazi privede do zloma konstrukcije. Lahko jo spremljamo in napovemo z elektrokemijskimi meritvami materiala ter s pravilnimi ukrepi zmanjšamo morebitno škodo. Enakomerna korozija na materialu je po navadi vidna že s prostim očesom, najpogosteje nastopi zaradi neustrezne površinske zaščite. Površina je zaradi tega podvržena delovanju oksidantov in korozivnega medija.

Jamičasta korozija[uredi | uredi kodo]
Jamičasta korozija v nasprotju z enakomerno korozijo deluje lokalizirano. Napade zelo majhne površine, pri čemer nastajajo bolj ali manj globoke jamice. Poškodbe materiala so precej večje kot pri splošni koroziji, saj so jamice pogosto prekurzorji razpok in zlomov v materialu, vodijo tudi do napetostnokorozijskega pokanja in medkristalne korozije. Je težko opazna, saj se korozijsko najbolj prizadeta območja nahajajo pod površino materiala.
Jamičasta korozija se po navadi pojavi v medijih z zelo visoko koncentracijo elektrolita. Elektrolit se preferenčno veže na določeno področje površine (defekt, razpoka), kjer spodbudi proces korozije. Pri tem nastane jamica, v kateri se vzpostavi visoka koncentracija korozijskih produktov, ki ne morejo sproti difundirati iz jamice. Zaradi koncentracijske razlike med zunanjo in notranjo raztopino nastane koncentracijski člen, ki še dodatno pospeši proces korozije.

Korozija v špranji[uredi | uredi kodo]
Mehanizem korozije v špranji je podoben mehanizmu jamičaste korozije. Tudi tu se vzpostavi koncentracijski člen, zaradi katerega poteka korozija. Korozija v špranji se pojavi pri stiku dveh površin (navoji, pritrdilne glave, podložke), med kateri se ujame del elektrolita. Notranjost špranje prevzame vlogo anode, iz katere se odtaplja kovina, na zunanji površini pa poteka redukcija korozivnih zvrsti, pogosto tudi kisika, če je ta prisoten v sistemu.

Galvanska korozija[uredi | uredi kodo]
Galvanska korozija je sicer bolj ali manj gonilna sila vseh tipov korozije, vendar o njej po navadi govorimo, kadar se med dvema deloma konstrukcije z različnimi kemijskimi in mikrostrukturnimi lastnostmi vzpostavi elektroprevodnost[5]. Pri tem del konstrukcije prevzame vlogo anode, ki korodira hitreje, del pa vlogo katode, ki korodira počasneje, kot posamezen del konstrukcije potopljen v korozivni medij. Korozijo povzroča potencialna razlika med materialoma.
Galvanska korozija ima neposredno zvezo z začetki elektrokemije; konec 18. stoletja je Luigi Galvani opravil naključni poizkus z žabjimi kraki in tako odkril galvanski člen.

Medkristalna korozija[uredi | uredi kodo]
Medkristalna korozija se pojavi na mejah med kristalnimi zrni v materialu. Pri kristalizaciji se na fazni meji koncentrirajo nečistoče, ki so pogosto korozijsko manj odporne kot čist material, iz česar je narejena konstrukcija. Medkristalna korozija je pogosta pri nerjavnih jeklih[6], v katerih je prisoten ogljik. Pri termični obdelavi jekla nastajajo karbidi (na primer CrC2), pri čemer se porabljajo korozijsko odpornejši elementi, nastane pa korozijsko manj odporen material.
Transkristalna (napetostna) korozija[uredi | uredi kodo]
Transkristalna (napetostna) korozija se pojavlja pri konstrukcijah, ki se nahajajo v korozivnem mediju in so pod stalno mehansko obremenitvijo. Predvsem vzdolž kristalnih zrn se pojavi krhki lom, ki posledično vodi do porušitve konstrukcije. Transkristalna korozija je ena izmed zahrbtnejših oblik korozije, saj so razpoke težko opazne, zato ga ni mogoče vnaprej napovedati.
Selektivno odtapljanje[uredi | uredi kodo]
Pri zlitinah je pogosta oblika korozije tudi selektivno odtapljanje. Med korozijskim procesom se en element iz zlitine hitreje odtaplja kot ostali elementi, pri čemer nastaja porozna struktura. Pri tem se poslabša trdnost materiala, izgubijo se tudi zaželene lastnosti površine.
Selektivno odtapljanje materiala se pogosto pojavlja pri medenini,[7][8] pri čemer se iz zlitine odtaplja cink, ostane pa porozna struktura bakra. Mehanizem korozije ni popolnoma znan, saj si raziskovalci niso enotni, ali se odtaplja zgolj cink ali pa se že raztopljeni baker ponovno izloči na elektrodo, pri čemer pa se dodatno porablja cink.
Zaščita materialov pred korozijo[uredi | uredi kodo]
Uspešen pristop k preprečevanju korozije se skriva v razumevanju najosnovnejših termodinamskih in kinetičnih principov. Za uspešen potek korozije so pomembni sledeči pogoji:
- anodna in katodna področja, med katerimi je omogočen pretok elektronov;
- raztopina, po kateri se gibljejo zvrsti, ki jih je mogoče reducurati ali oksidirati;
- ustrezna površina, na kateri poteka prenos elektronov med materialom in zvrstmi v raztopini.
Na potek korozije lahko vplivamo, če spremenimo katerega izmed naštetih dejavnikov.
Vpliv materiala na potek korozije[uredi | uredi kodo]
Ustrezna izbira materiala ima pomemben vpliv na potek korozije. Njegove kemijske lastnosti namreč določajo spekter kemijskih reakcij, ki potekajo ob stiku s korozivnim medijem. V splošnem želimo, da izbrani material čim manj reagira z okolico in na tak način preprečimo korozijski proces.
Kovine z višjim elektrokemijskim potencialom od vodikovega v kislih medijih ne korodirajo, saj redukcija H+ ionov do vodika ne poteka. Kovini lahko elektrodni potencial spremenimo in na tak način zmanjšamo hitrost korozije. Najbolj običajno je, da potencial znižamo glede na korozijskega in s tem povečamo katodni tok. Katodno zaščito lahko izvedemo na dva načina, in sicer z metodo darujoče elektrode in z metodo vzbujenega toka.
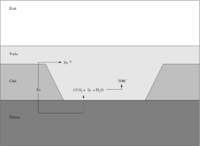
Pri metodi darujoče elektrode zgradimo elektrokemijsko celico s pritrditvijo anod na izbrana mesta kovinske konstrukcije, ki jih želimo zaščititi. Pri tem darujoča elektroda prevzame vlogo anode in se tekom korozije raztaplja ter ohranja lastnosti konstrukcije.
Pri metodi vzbujenega toka namesto darujoče elektrode uporabimo zunanji vir napetosti, vendar je princip delovanja enak. Na materialu, ki ga želimo zaščititi vzbujamo majhen katodni tok, medtem ko inertna elektroda prevzame vlogo anode, na kateri se oksidirajo zvrsti v raztopini.
Poleg materiala ima pomembno vlogo oblika konstrukcije. Z uporabo gladkih (ali celo poliranih) materialov zmanjšamo površino, na kateri poteka korozija. V dinamičnih sistemih so zaželene oblike, ki omogočajo čim bolj nemoten pretok, saj trenje med tekočino in stenami konstrukcije dodatno pospešuje proces korozije.
Vpliv raztopine na potek korozije[uredi | uredi kodo]

Raztopina, ki obdaja konstrukcijo, je poleg materiala tisti del sistema, v katerem lahko potekajo kemijske spremembe. Korozijski proces se ustavi, če se zaustavijo nezaželene kemijske reakcije v raztopini. To se najpogosteje doseže s spremembo sestave raztopine:
- raztopljeni kisik se odstrani s prepihovanjem z dušikom ali dodatkom hidrazina;
- kisle oziroma alkalne raztopine se nevtralizira;
- agresivne ione se odstrani z ionsko izmenjavo in osmozo ali se zmanjša njihova koncentracijo z razredčenjem oziroma tvorbo stabilnih kompleksov;
- vlažnost sistema se zmanjša s prezračevanjem, povišanjem temperature ali dodatkom adsorbenta za vlago.
če imamo možnost, za izbrani sistem že na začetku izberemo ustreznejšo raztopino. Prisotnost fosfatov in kromatov v raztopini izboljša korozijsko odpornost nekaterih vrst jekel.
Vpliv fazne meje na potek korozije[uredi | uredi kodo]
Kemijske reakcije pri koroziji v glavnem potekajo na fazni meji med materialom in raztopino. Glede na to, da je večina reakcij elektrokemijske narave, jih lahko zaustavimo, če onemogočimo prenos elektronov preko fazne meje ali če preprečimo dostop ionov oziroma molekul do površine. Na površini želimo ustvariti oviro, preko katere je onemogočen prehod tako elektronov kot tudi reaktivnih zvrsti.

Pri anodni zaščiti na površini tvorimo pasivno plast (po navadi je to oksidni film), s katero kovino zaščitimo pred korozijskimi procesi. Plast preprečuje difuzijo reaktivnih zvrsti do površine materiala, zato je električni tok v nekem intervalu neodvisen od napetosti. Pri določeni napetosti pride do preboja pasivne plasti, pri čemer se poruši korozijska zašcita. Na tak način je mogoče zaščititi nikelj, aluminij, titan, molibden, krom in večino zlitin, ki vsebujejo naštete elemente.
Inhibitorji so organski ali anorganski dodatki, ki upočasnijo proces korozije. V korozijski sistem jih dodajamo v manjših količinah. Glede na področje delovanja jih delimo na anodne, katodne in splošne. Inhibitorji se preferenčno adsorbirajo na površino materiala in s tem preprečijo dostop reaktivnih zvrsti do površine.

Z nanosom prevlek na površino material izoliramo od okolja in ustavimo korozijo. Izbira možnih prevlek je velika in nam omogoča uporabo cenejših materialov z želenimi mehanskimi lastnostmi. Sem sodijo barvne, plastične in kovinske prevleke, različni premazi, emajli, beton. Zaradi velike obremenitve na okolje se pri korozijski zaščiti pojavljajo težnje po čim bolj neškodljivih in činkovitih rešitvah, ki pogosto mejijo na področje zelene kemije.
Glej tudi[uredi | uredi kodo]
Opombe in sklici[uredi | uredi kodo]
- ↑ Positive and negative aspects of sulphate-reducing bacteria in environment and industry
- ↑ »arhivska kopija«. Arhivirano iz prvotnega spletišča dne 26. avgusta 2010. Pridobljeno 24. junija 2010.
- ↑ Za kratko izpeljavo Nernstove enačbe poglej pogovorno stran. Korozija, pogovorna stran
- ↑ Za kratko izpeljavo Butler-Volmerjeve poglej pogovorno stran. Korozija, pogovorna stran
- ↑ http://corrosion-doctors.org/Forms-galvanic/galvanic-corrosion.htm
- ↑ http://corrosion-doctors.org/Forms-intergranular/intergranular.htm
- ↑ http://corrosion-doctors.org/Forms-selective/dealloy.htm
- ↑ Corrosion of cold-deformed brass in acid sulphate solution
Viri[uredi | uredi kodo]
- J. O' M. Bockriss, A. & Reddy, K.N. (1998). Modern Electrochemistry Vol. 1, Ionics, 2. izdaja. New York: Plenum Press. (COBISS)
- J. O' M. Bockriss, A. & Reddy, K.N. (2000). Modern Electrochemistry Vol. 2a, Fundamentals of electrodics, 2. izdaja. New York: Plenum Press. (COBISS)
- J. O' M. Bockriss, A. & Reddy, K.N. (2000). Modern Electrochemistry Vol. 2b, Electrodics in chemistry, engineering, biology, and environmental science, 2. izdaja. New York: Plenum Press. (COBISS)
- Kortum, G. (1948). Lehrbuch der Elektrochemie. Wiesbaden: Dietrich'Sche Verlagsbuchhandlung.
- D. R. Crow (1994). Principles and applications of electrochemistry, 4. izdaja, Stanley Thorens. (COBISS)
- P. Marcus (2002). Corrosion mechanisms in theory and practice, 2. izdaja, New York: Marcel Dekker. (COBISS)
- T. Kosec, I. Milošev, Korozijski procesi, vrste korozije in njihove zaščite, Vakuumist (2004) [1]
- Corrosion Doctors






















