Etilenglikol

| |||
| |||

| |||
| Imena | |||
|---|---|---|---|
| IUPAC ime
etan-1,2-diol
| |||
| Druga imena
1,2-etandiol
1,2-dihidroksietan
glikol | |||
| Identifikatorji | |||
| |||
3D model (JSmol)
|
|||
| 3DMet | |||
| Kratice | MEG | ||
| 505945 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.159 | ||
| EC število |
| ||
| Gmelin | 943 | ||
| KEGG | |||
| MeSH | Ethylene+glycol | ||
PubChem CID
|
|||
| RTECS število |
| ||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Lastnosti | |||
| C2H6O2 | |||
| Molska masa | 62,07 g·mol−1 | ||
| Videz | bistra, brezbarvna tekočina | ||
| Gostota | 1,1132 g/cm³ | ||
| Tališče | −12,9 °C (8,8 °F; 260,2 K) | ||
| Vrelišče | 197,3 °C (387,1 °F; 470,4 K) | ||
| mešljiv z vodo | |||
| Topnost | topen v večini organskih topil | ||
| Viskoznost | 1,61 × 10−2 N*s / m2[1] | ||
| Nevarnosti | |||
| Glavne nevarnosti | Zelo škodljiv za otroke in domače živali. Pri zaužitju nemudoma poiskati zdravniško pomoč. | ||
EU klasifikacija (DSD) (zastarelo)
|
Zdravju škodljivo (Xn) | ||
| R-stavki (zastarelo) | R22 R36 | ||
| S-stavki (zastarelo) | S26 S36 S37 S39 (S45) S53 | ||
| NFPA 704 (diamant ognja) | |||
| Plamenišče | v zaprti posodi 111 °C (232 °F; 384 K) | ||
| Sorodne snovi | |||
| Sorodno dioli | propilenglikol dietilenglikol trietilenglikol polietilenglikol | ||
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |||
| Sklici infopolja | |||
Etilenglikol (IUPAC ime: etan-1,2-diol) je organska spojina s formulo (CH2OH)2. Uporablja se predvsem kot surovina za proizvodnjo poliesterskih vlaken in plastenk (PET) in sredstvo proti zmrzovanju, na primer v hladilnih tekočinah za avtomobile. Je strupena brezbarvna viskozna tekočina sladkega okusa. Z njim se najpogosteje zastrupijo male živali, ki ližejo hladilno tekočino, izteklo iz vozil.[2]
Proizvodnja[uredi | uredi kodo]
Industrijska proizvodnja[uredi | uredi kodo]
Etilenglikol se proizvaja iz etilena (etena, CH2=CH2) preko vmesnega produkta etilen oksida (CH2-O-CH2). V kemijski reakciji etilen oksida z vodo nastane etilenglikol:
- CH2-O-CH2 + H2O → HO–CH2CH2–OH
Reakcijo katalizirajo kisline ali baze, poteka pa tudi pri nevtralnem pH pri povišanih temperaturah. Najvišji izkoristki (okoli 90%) se dosežejo pri kislem ali nevtralnem pH in velikem prebitku vode. Glavni stranski produkti so oligomeri dietilenglikol, trietilenglikol in tetraetilenglikol. Ločitev oligomerov in vode od glavnega proizvoda je energijsko zahteven postopek. Letna proizvodnja etilenglikola je okoli 6,7 milijona ton.[2]
Večjo selektivnost se doseže s Shellovim OMEGA postopkom, v katerem se etilen oksid najprej z ogljikovim dioksidom (CO2) pretvori v etilen karbonat. Slednji se nato v drugem koraku hidrolizira z bazičnim katalizatorjem v 98 % monoetilenglikol.[3] Ogljikov dioksid, ki nastaja kot stranski produkt, se vrača v proizvodni proces. Del primarnega ogljikovega dioksida prihaja iz proizvodnje etilen oksida, v kateri del etilena popolnoma oksidira.
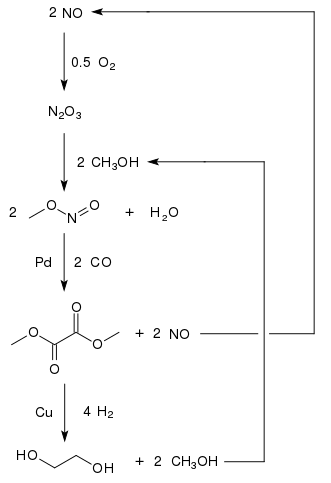
V državah z velikimi rezervami premoga in manj strogo okoljsko regulativo se etilen glikol proizvaja iz ogljikovega monoksida (CO). Obetajoč pristop kaže oksidstivna karbonilacija metanola v etilenglikol.[4] V etilenglikol se lahko z visokimi izkoristki (94,7%)[5] pretvori tudi dimetil oksalat s hidrogeniranjem z bakrovim katalizatorjem:[6]
Metanol se reciklira, torej se porabljajo samo ogljikov monoksid, vodik in kisik. Tovarna s proizvodnjo 200.000 ton etilenglikola letno je v Notranji Mongoliji. Druga tovarna s kapaciteto 250.000 ton letno je v kitajski provinci Henan.[7] Na Kitajskem se je leta 2015 načrtovala gradnja še 17 podobnih tovarn.[8]
Biološki procesi[uredi | uredi kodo]
Gosenica velikega voščenega molja (Galleria mellonella) ima v črevesni flori mikroorganizme, ki razgradijo polietilen (PE) v etilenglikol.[9][10][11]
Molekule etilenglikola so opazili tudi v vesolju.[12]
Zgodovinski postopki[uredi | uredi kodo]
Po večini virov je etilenglikol prvi sintetiziral francoski kemik Charles-Adolphe Wurtz (1817–1884) leta 1856.[13] V prvem koraku je etilen jodid (C2H4I2) obdelal s strebrovim acetatom (CH3-COOAg) in nastali diacetat hidroliziral s kalijevim hidroksidom. Wurtz je nastali produkt imenoval "glikol", ker je imel lastnosti etanola in glicerola (s tremi hidroksilnimi skupinami).[14] Leta 1859 je pripravil etilenglikol s hidriranjem etilenoksida.[15] Zdi se, da pred prvo svetovno vojno ni bilo industrijske proizvodnje ali uporabe etilen glikola, ko so v Nemčiji razvili njegovo sintezo iz etilen diklorida, pa se je začel uporabljati v industriji eksplozivov kot nadomestek za glicerol.
V Združenih državah Amerike se je začela leta 1917 polindustrijska proizvodnja etilenglikola iz etilenklorhidrina. Industrijska proizvodnja se je začela leta 1925 v Južnem Charlestonu v Zahodni Virginiji (Carbide and Carbon Chemicals Co., zdaj Union Carbide Corp.). Do leta 1929 so skoraj ves etilenglikol porabili proizvajalci dinamita. Leta 1937 je stekla proizvodnja po tako imenovanem Lefortovem postopku, v katerem se etilen v plinski fazi oksidira v etilen oksid. Union Carbide je obdržal monopol nad tem postopkom do leta 1953.
Uporaba[uredi | uredi kodo]
Večina etilenglikola se porabi v antifrizih in hladilnih tekočinah, odpornih proti zmrzovanju (50%), in kot surovina za proizvodnjo poliestrov, na primer polietilen tereftalata (PET) (40%).[2]
Hladilno sredstvo in sredstvo za prenos toplote[uredi | uredi kodo]
Več kot polovica etilenglikola se porabi kot medij za prenos toplote, na primer v avtomobilih za hlajenje motorja in vodno hlajenih računalnikih. V vodnih raztopinah se pogosto uporablja v klimatskih sistemih z zunanjimi hladilniki in sistemih, ki morajo delovati pod zmrziščem vode. V geotermalnih ogrevalnih/hladilnih sistemih je etilenglikol medij, ki prenaša toploto iz geotermalnega vira (jezero, ocean, vodnjak…) do toplotne črpalke ali obratno, če gre za hlajenje.
Specifična toplota čistega etilenglikola je približo pol manjša od specifične toplote vode, zato so manjše tudi specifične toplote njegovih vodnih raztopin. Zmes glikola in vode v razmerju 1:1 ima specifično toploto približno 3140 J/(kg•°C), se pravi tri četrtine specifične toplote vode. Pretok hladilne tekočine mora biti zato temu primerno večji.
Antifriz[uredi | uredi kodo]
Čisti etilenglikol zmrzne pri približno −12 °C, v mešanicah z vodo pa pri nižjih temperaturah. Zmes 60% etilenglikola in 40% vode zmrzne pri −45 °C.[2] Podobno se obnaša tudi dietilenglikol. Znižanje zmrzišča zelo razredčenih raztopin se lahko razloži s koligativnimi lastnostmi raztopin, v zelo koncentriranih raztopinah, kakršni so je antifrizi, pa se odstopanje od idealno raztopine lahko razloži z vplivom medmolekularnih sil.
Mešalna razmerja so odvisna od tega, ali se uporablja etilenglikol ali propilenglikol. Za etilenglikol sta tipični mešalni razmerji 30/70 in 35/65, za propilenglikol pa 35/65 and 40/60. Pomembno je da tekočina ne zmrzne niti pri najnižji delovni temperaturi.[16]
Zaradi pojava znižanja tališča se etilenglikol uporablja tudi kot sredstvo za odmrzovanje na primer avtomobilskih in letalskih stekel in v sredstvih za preprečevanja kristalizacije vode v bioloških tkivih in organih.
Razen tega, da etilenglikol znižuje tališče vodnih raztopin, tudi zvišuje njihova vrelišča. Tempereturno delovno območje raztopin je zato večje od delovnega območja vode. Vzrok za oba pojava je znižanje parnega tlaka vode, ki je značilno za večino binarnih raztopin.
Predhodnik polimerov[uredi | uredi kodo]

V industriji plastike je etilenglikol pomemben predhodnik poliestrskih vlaken in smol. Polietilentereftalat se uporablja za plastenke za brezalkoholne pijače.
Druga raba[uredi | uredi kodo]
Sušilno sredstvo[uredi | uredi kodo]
V industriji naravnega plina se etilenglikol v približno enakih količinah kot trietilenglikol (TEG) uporablja za odstranjevanje vlage iz naravnega plina pred nadaljnjim procesiranjem.
Inhibitor hidriranja[uredi | uredi kodo]
Etilenglikol se v dolgih večstopenjskih plinovodih naravnega plina uporablja kot inhibitor tvorbe hidratov. Med končnim čiščenjem naravnega plina se etilenglikol izloči in se po odstranitvi vode in anorganskih soli ponovno uporabi.
Vlaga se iz naravnega plina odstranjuje tako, da v izpiralnem stolpu od zgoraj navzdol vbrizgava etilenglikol, od spodaj navzgor pa vpihava vlažen naravni plin. Iz vrha stolpa izhaja brezvodni plin. Etilenglikol se regenerira in vrača v proces.
Razen za odstranjevanje vlage se etilenglikol uporablja tudi za znižanje temperature, pri kateri nastajajo hidrati. Čistost etilenglikola za zniževanje temperature tvorbe hidratov je običajno okoli 80%, medtem ko je čistost za odstranjevanje vode običajno 95 do več kot 99%. Hitrost vbrizgavanja etilenglikola za znižanje temperature nastajanja hidratov je mnogo nižja od hitrosti vbrizgavanja v stolpih za odstranjevanje vlage.
Nišne aplikacije[uredi | uredi kodo]
Manjše količine etilenglikola se porabijo v industriji kondenzatorjev, za sintezo 1,4-dioksana, kot dodatek za preprečevanje korozije v tekočinskih hladilnih sistemih osebnih računalnikov in v lečah katodnih cevi televizijskih aparatov z zadnjo projekcijo. Uporablja se tudi v proizvodnji nekaterih cepiv, v cepivih samih pa ga ni. V majhnih količinah je v pastah za čevlje (1-2 %) in nekaterih črnilih in barvilih. Nekaj se ga porabi tudi za preventivno ali kurativno zaščito lesa pred gnitjem in trohnenjem, predvsem muzejskih predmetov in celo lesenih čolnov, ker je relativno poceni. V manjših koncentracijah je v čistilih za stekla, katerih glavna sestavina je izopropil alkohol. Etilenglikol se običajno uporablja kot konzervans za biološka vzorce, zlasti v srednjih šolah med seciranjem, ker je varnejši od formaldehida. Uporablja se tudi kot sestavina hidravličnih tekočin na vodni osnovi, namenjenih za nadzor podvodne opreme za proizvodnjo nafte in plina.
V organskih sintezah se uporablja kot zaščitna skupina za karbonilne spojine (aldehidi, ketoni).[17]
Silicijev dioksid reagira v vročen refluksu v dušikovi atmosferi z etilenglikolom in bazo alkalijske kovine in tvori zelo reaktivne pentakoordinirane silikate, ki omogočajo sintezo različnih novih silicijevih spojin.[18] Silikati so praktično netopni v vseh polarnih topilih, razen v metanolu.
Kemijske reakcije[uredi | uredi kodo]
Etilenglikol se uporablja kot zaščitna skupina za karbonilne skupine v organskih sintezah. Obdelava ketonov ali aldehidov z etilenglikolom v prisotnosti kislega katalizatorja (npr. p-toluenesulfonska kislina, BF3•Et2O) daje odovarjajoči 1,3-dioksalan, ki je odporen na baze in druge nukleofile. 1,3-dioksalansko skupino se zato zlahka odstrani z naknadno kislo hidrolizo.[19] V prikazanem primeru je bil izoforon zaščiten z etilenglikolom s p-toluensulfonsko kislino z zmernim izkoristkom. Voda se je odstranjevala za azeotropsko destilacijo, da bi se ravnotežje pomaknilo v desno.[20]

Strupenost[uredi | uredi kodo]
Etilenglikol je zelo strupen ob zaužitju. Za človeka je oralni LDLo = 786 mg / kg.[21] Nevaren je predvsem zaradi sladkega okusa, ki privlači otroke in živali. Po zaužitju se oksidira v glikolsko kislino, ta pa v oksalno kislino, ki je strupena. Kislina in njeni stranski produkti najprej napadejo centralni živčni sistem, zatem srce in nazadnje ledvica. Nezdravljene zastrupitve se lahko končajo s smrtjo.[22]
Znaki zastrupitve[uredi | uredi kodo]
Znaki zastrupitve so slabost, bruhanje, bolečine v trebuhu, tetanija (hipokalcemija) in, hiperpnea (težka metabolična acidoza). Do smrti pride običajno zaradi zastoja dihanja ali kardiocirkulacijske odpovedi. Če zastrupljenec preživi začetno fazo, pride do akutne ledvične insuficience z vsemi mogočimi zapleti.
Prva pomoč[uredi | uredi kodo]
Bruhanja se ne sme izzivati! Zastrupljenec mora spiti nekaj kozarcev vode. Če pride do spontanega bruhanja, mora zastrupljenec izprati usta z vodo ter popiti 1-2 decilitra vode. Zastrupljenec mora takoj popiti 1,5 do 2 decilitra močne alkoholne pijače, na primer žganja, ter poiskati zdravniško pomoč. Če pot do zdravnika traja dlje časa, mora zastrupljenec vsake pol ure popiti še 0,1 decilitra alkoholne pijače.[23]
Varni nadomestki za etilen glikol[uredi | uredi kodo]
Na tržišču so dostopni antifrizi za avtomobile, ki namesto etilenglikola vsebujejo propilenglikol. Na splošno veljajo za bolj varne, ker propilen glikol ni tako okusen[note 1] in se v telesu pretvori v mlečno kislino, ki je normalen produkt metabolizma.[26]
Avstralija, Združeno kraljestvo in nekaj ameriških zveznih držav je leta 2012 zahtevalo, sa se antifrizu doda snov z grenkim okusom (denatonijev benzoat). Decembra 2012 so proizvajalci antifriza v ZDA začeli prostovoljno dodajati denatonijev benzoat v vse antifrize, ki se prodajajo na ameriškem trgu.[27]
Vpliv na okolje[uredi | uredi kodo]
Etilenglikol je kemikalija, ki se proizvaja v zelo velikih količinah. Na zraku se razgradi v 10 dneh, v vodi in zemlji pa v nekaj tednih. V naravo pride s škropljenjem produktov, ki vsebujejo etilenglikol. To se dogaja predvsem na letališčih, kjer se uporablja za odstranjevanje ledu z letal.[28] Majhni odmerki etilenglikola tudi v daljšem času niso strupene, so veliki odmerki (≥ 1000 mg/kg na dan) teratogeni.
Pri miših in podganah se pri vseh oblikah vnosa etilenglikola pojavijo okvare okostja in spačenost.[29]
Opomba[uredi | uredi kodo]
- ↑ Čisti propilen glikol nima grenkega okusa. Pogosto je uporablja kot aditiv v prehranskih proizvodih, na primer v zamrzovanju peciv in za povečanje skladiščne trajnosti stepene smetane. Industrijski propilenglikol je zaradi nečistoč običajno rahlo grenkega ali kiselkastega okusa. V Merckovem Indexu niti etilenglikol[24] niti propilenglikol[25] nista opisana kot grenka.
Sklici[uredi | uredi kodo]
- ↑ Elert, Glenn. »Viscosity«. The Physics Hypertextbook. Pridobljeno 2. oktobra 2007.
- ↑ 2,0 2,1 2,2 2,3 Siegfried Rebsdat, Dieter Mayer. "Ethylene Glycol". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a10_101.
- ↑ Scott D. Barnicki. "Synthetic Organic Chemicals". V Handbook of Industrial Chemistry and Biotechnology (ur. James A. Kent). New York: Springer, 2012. 12th ed. ISBN 978-1-4614-4259-2.
- ↑ Nexant/Chemsystems. "Coal to MEG, Changing the Rules of the Game"(PDF). Arhivirano iz izvirnika 14. julija 2011. Pridobljeno 8. avgusta 2016.
- ↑ 983 EP 046 983, S. Tahara in drugi. "Process for continuously preparing ethylene glycol", assigned to Ube Industries and H. T. Teunissen and C. J. Elsevier, Ruthenium catalyzed hydrogenation of dimethyl oxalate to ethylene glycol, J. Chem. Soc., Chem. Commun., 1997, 667–668). DOI:10.1039/A700862G.
- ↑ S. Zhang in drugi. Highly-Dispersed Copper-Based Catalysts from Cu–Zn–Al Layered Double Hydroxide Precursor for Gas-Phase Hydrogenation of Dimethyl Oxalate to Ethylene Glycol. Catalysis Letters, Sept. 2012, 142 (9), 1121–1127. DOI:10.1007/s10562-012-0871-8.
- ↑ [1]
- ↑ Gräbner, Martin (24. november 2014). Industrial Coal Gasification Technologies Covering Baseline and High-Ash Coal. ISBN 9783527336906.
- ↑ Yang, Jun; Yang, Yu; Wu, Wei-Min; Zhao, Jiao; Jiang, Lei (2014-12-02). "Evidence of polyethylene biodegradation by bacterial strains from the guts of plastic-eating waxworms". Environmental Science & Technology. 48 (23): 13776–13784. Bibcode: 2014EnST...4813776Y.doi:10.1021/es504038a. ISSN 1520-5851. PMID 25384056.
- ↑ Bombelli, Paolo; Howe, Christopher J.; Bertocchini, Federica (24. april 2017). "Polyethylene bio-degradation by caterpillars of the wax moth Galleria mellonella". Current Biology. 27 (8): R292–R293.Bibcode:1996CBio....6.1213A. doi:10.1016/j.cub.2017.02.060.hdl:10261/164618. ISSN 0960-9822. PMID 28441558.
- ↑ Khan, Amina (24. april 2017). "Stubborn plastic may have finally met its match: the hungry wax worm". Los Angeles Times. Pridobljeno 25. aprila 2017.
- ↑ Hollis, J.M.; Lovas, F.J.; Jewell, P.R.; Coudert, L.H. (20. maj 2002). »Interstellar Antifreeze: Ethylene Glycol«. The Astrophysical Journal. 571 (1): L59–L62. Bibcode:2002ApJ...571L..59H. doi:10.1086/341148.
- ↑ Adolphe Wurtz (1856). "Sur le glycol ou alcool diatomique". Comptes Rendus. 43: 199–204.
- ↑ Wurtz (1856), str. 200.
- ↑ Wurtz (1859). Comptes rendus, 49: 813–815.
- ↑ [2]
- ↑ "Ethylene glycol acetal". The Organic Synthesis Archive. synarchive.com.
- ↑ Laine, Richard M.; Blohowiak, Kay Youngdahl; Robinson, Timothy R.; Hoppe, Martin L.; Nardi, Paola; Kampf, Jeffrey; Uhm, Jackie (17. oktober 1991). "Synthesis of pentacoordinate silicon complexes from SiO2"(PDF). Nature. 353 (353): 642–644. Bibcode: 1991Natur.353..642L. doi: 10.1038/353642a0..
- ↑ "Statement of the Science Report for Ethylene Glycol". 3.3.2.2 Non-neoplastic effects. Health Canada www.hc-sc.gc.ca. 24. junij 2013. Pridobljeno 27. avgusta 2014.
- ↑ J. M. Hollis; F. J. Lovas; P. R. Jewell; L. H. Coudert (2002-05-20). "Interstellar Antifreeze: Ethylene Glycol". The Astrophysical Journal. 571 (1): L59–162. Bibcode: 2002ApJ...571L..59H. doi: 10.1086/341148.
- ↑ Safety Officer in Physical Chemistry (November 23, 2009). "Safety (MSDS) data for ethylene glycol". Oxford University. Pridobljeno 30. decembra 2009.
- ↑ Ethylene glycol. National Institute for Occupational Safety and Health. Emergency Response Database. 22. avgust 2008. Pridobljeno 31. decembra 2008.
- ↑ Chemius. Varnostni list: Antifriz NF. Revidirano 19. marca 2018. Pridobljeno 21. februarja 2021.
- ↑ The Merck Index (15th ed.). Royal Society of Chemistry. 2013. str. M5122.
- ↑ The Merck Index (15th ed.). Royal Society of Chemistry. 2013. str. M9238.
- ↑ Pieter Klapwijk (27. januar 2010). "Ethylene Glycol Poisoning" Arhivirano 2013-01-26 na Wayback Machine.. The Rested Dog Inn. Pridobljeno 11. oktober 2012.
- ↑ "Antifreeze and Engine Coolant Being Bittered Nationwide". Consumer Specialty Products Association. 13. december 2012. Athivirano iz izvirnika 28. decembra 2012. Pridobljeno 30. junija 2016.
- ↑ CDC ToxFAQs.
- ↑ "Statement of the Science Report for Ethylene Glycol". 3.3.2.2 Non-neoplastic effects. Health Canada www.hc-sc.gc.ca. 24. junij 2013. Pridobljeno 27. avgusta 2014.