Hidroksilni radikal

| |
| Imena | |
|---|---|
| IUPAC ime
Hidroksilni radikal
| |
| Identifikatorji | |
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| Gmelin | 105 |
| KEGG | |
PubChem CID
|
|
CompTox Dashboard (EPA)
|
|
| |
| |
| Lastnosti | |
| HO | |
| Molska masa | 17,01 g·mol−1 |
| Termokemija | |
| Standardna molarna entropija S |
183.71 J K−1 mol−1 |
Std tvorbena
entalpija (ΔfH⦵298) |
38.99 kJ mol−1 |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |

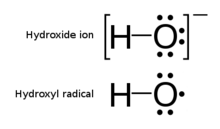
Hidroksilni radikal •OH je nevtralna oblika hidroksidnega iona (OH−). Hidroksilni radikali so izredno reaktivni (zlahka postanejo hidroksilna skupina) in posledično kratkoživi; vendar pa so pomemben sestavni del radikalske kemije.[1] Nastanejo predvsem z razgradnjo hidroperoksidov (ROOH) ali v atmosferski kemiji z reakcijo med vzburjenim atomarnim kisika in vodo. Je tudi pomemben radikal v jedrski kemiji, saj vodi do nastanka vodikovega peroksida in kisika, ki lahko povečata korozijo v hladilnih sistemih, izpostavljenih radioaktivnem sevanju. Hidroksilni radikali nastajajo tudi pri razpadu H2O2 zaradi UV-sevanja (predlagano leta 1879) in verjetno v Fentonovi reakciji, kjer sledovi reduciranih prehodnih kovin katalizirajo preko peroksida posredovano oksidacijo organskih spojin.
V organski sintezi so hidroksilni radikale najpogosteje tvori s fotolizo 1-hidroksi-2(1H)-piridinetiona (na sliki).
Hidroksilni radikal pogosto imenujemo tudi "čistilo" troposfere, ker tam reagira z veliko škodljivimi snovmi. Razgrajuje jih s "krekingom", ki je pogosto prvi korak pri njihovi odstranitvi. Pomembno vlogo ima tudi pri odpravljanju nekaterih toplogrednih plinov, kot sta metan in ozon.[2] Hitrost reakcije s hidroksilnim radikalom pogosto določa, kako dolgo se škodljiva snov zadržuje v ozračju, če ni prej podvržena fotolizi ali je ne izpere dež. Metan, ki reagira relativno počasi, ima povprečno življenjsko dobo nad 5 leti, veliko različnih CFC pa celo 50 let ali več. Drugi onesnaževalci, kot so večji ogljikovodiki, so lahko odstranjeni že v nekaj urah
Prva reakcija mnogih hlapnih organskih spojin je odstranitev vodikovega atoma; tvori se vodo in alkilni radikal (R•):
- •OH + RH → H2O + R•
Alkilni radikali običajno hitro reagirajo s kisikom; tvori se peroksi radikal:
- R• + O2 → RO•
2
Usoda tega radikala v troposferi je odvisna od dejavnikov kot so količina sončne svetlobe, onesnaženost v ozračju in narava alkilnega radikala, iz katerega je nastal.[3]
Biološki pomen
[uredi | uredi kodo]Hidroksilni radikali nastajajo občasno kot stranski produkt imunske dejavnosti. Makrofagi in celice mikroglije najpogosteje tvorijo to spojino kot odgovor na določene povzročitelje bolezni, kot so nekatere bakterije. Uničujoče delovanje hidroksilnih radikalov je bilo povezano z več nevrološkimi avtoimunskimi boleznimi, kjer so imunske celice prekomerno aktivirane in postanejo strupene za sosednje zdrave celice.[4]
Hidroksilni radikal lahko poškoduje skoraj vse vrste makromolekul: ogljikove hidrate, nukleinske kisline (mutacije), lipide (lipidna peroksidacija) in aminokisline (npr. pretvorba fenilalanina v m-tirozinn o-tirozin).[5] Hidroksilni radikal ima zelo kratek in vivo razpolovni čas (približno 10-9 sekund) in visoko reaktivnost.[6] Zaradi tega je zelo nevaren za organizem.[7][8]
Za razliko od superoksidaa, ki ga lahko odstranjuje encim superoksid-dismutaza, hidroksilnih radikalov ni mogoče odpraviti z encimsko reakcijo.
Uporaba pri čiščenju vode
[uredi | uredi kodo]Hidroksilni radikali igrajo ključno vlogo pri oksidativnem uničenju organskih onesnaževalcev z vrsto metodologij, skupno znanih kot napredni oksidacijski procesi ("advanced oxidation processes" ali AOP-ji). Uničenje škodljivih snovi z AOP-ji temelji na neselektivnih reakcijah hidroksilnih radikalov na organskih spojinah. Ta proces je zelo učinkovit proti vrsti onesnaževalcev, vključno s pesticidi, farmacevtskimi spojinami, barvili, itd.[9][10]
Pomen v Zemljini atmosferi
[uredi | uredi kodo]Hidroksilni radikal •OH je eden glavnih kemijskih zvrsti za nadzor oksidativne kapacitete Zemljine atmosfere, kjer vpliva na koncentracijo in porazdelitev toplogrednih plinov in škodljivih snovi. Je najbolj razširjen oksidant v troposferi, najnižjem delu atmosfere. Razumevanje variabilnosti •OH je pomembno pri vrednotenju vplivov človeka na ozračje in podnebje. Zvrst •OH ima v atmosferi življenjsko dobo krajšo od sekunde.[11] Razumevanja vloge •OH v procesu oksidacije metana (CH4) v ozračju, najprej v ogljikov monoksid (CO) in nato v ogljikov dioksid (CO2), je pomembno za ocenjevanje časa zadrževanja tega toplogrednega plina, skupni "ogljikov proračun" troposfere in njegov vpliv na proces globalnega segrevanja. Življenjska doba •OH v Zemljini atmosferi je kratka, zato so koncentracije •OH v zraku zelo nizke; za njegovo neposredno zaznavanje so potrebne zelo občutljive metode.[12] Svetovno povprečje koncentracije hidroksilnih radikalov so bile izmerjene posredno z analizo metilkloroforma (CH3CCl3), prisotnega v zraku. Iz rezultatov[13] je razvidno, da je medletna variabilnost v koncentraciji •OH, ocenjena iz meritev CH3CCl3, majhna, kar pomeni, da je globalni •OH na splošno dobro pufran pred motnjami. Ta majhna variabilnost je skladna z meritvami metana in drugih plinov v sledeh, ki jih povečini oksidira •OH, kot tudi z globalimi izračuni fotokemičnih modelov.
V letu 2014 so raziskovalci poročali o odkritu "luknje" oz. odsotnosti hidroksilnih radikalov preko celotne globine troposfere na velikem območju tropskega zahodnega Tihega oceana. Domnevajo, da ta luknja omogoča uhajanje velike količine kemikalij, ki uničujejo ozon, v stratosfero, in da to lahko precej krepi tanjšanje ozonskega plašča v polarnih regijah, s čimer ima potencialno velike posledice za Zemljino podnebje.[14]
Reference
[uredi | uredi kodo]- ↑ Hayyan M.; Hashim M.A.; AlNashef I.M. (2016). »Superoxide Ion: Generation and Chemical Implications«. Chem. Rev. 116 (5): 3029–3085. doi:10.1021/acs.chemrev.5b00407.
- ↑ »Trends in the Hydroxyl Free Radical« (PDF) (IPCC AR4 WG1). IPCC.
The hydroxyl free radical (OH) is the major oxidizing chemical in the atmosphere, destroying about 3.7 Gt of trace gases, including CH4 and all HFCs and HCFCs, each year (Ehhalt, 1999).
{{navedi časopis}}: Sklic journal potrebuje|journal=(pomoč) - ↑ (See chapters 12 & 13 in External Links "University Lecture notes on Atmospheric chemistry)
- ↑ Kincaid-Colton, Carol; Wolfgang Streit (november 1995). »The Brain's Immune System«. Scientific American.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ PubMed.
- ↑ Sies, Helmut (Marec 1993). »Strategies of antioxidant defense«. European Journal of Biochemistry. 215 (2): 213–219. doi:10.1111/j.1432-1033.1993.tb18025.x. PMID 7688300.
- ↑ Reiter RJ, Melchiorri D, Sewerynek E, in sod. (Januar 1995). »A review of the evidence supporting melatonin's role as an antioxidant«. J. Pineal Res. 18 (1): 1–11. doi:10.1111/j.1600-079x.1995.tb00133.x. PMID 7776173.
- ↑ Reiter RJ, Carneiro RC, Oh CS (Avgust 1997). »Melatonin in relation to cellular antioxidative defense mechanisms«. Horm. Metab. Res. 29 (8): 363–72. doi:10.1055/s-2007-979057. PMID 9288572.
- ↑ Sunil Paul, M. M.; Aravind, Usha K.; Pramod, G.; Aravindakumar, C.T. (april 2013). »Oxidative degradation of fensulfothion by hydroxyl radical in aqueous medium«. Chemosphere. Zv. 91, št. 3. str. 295–301. Bibcode:2013Chmsp..91..295S. doi:10.1016/j.chemosphere.2012.11.033. PMID 23273737. Pridobljeno 2. decembra 2013.
{{navedi revijo}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ »Oxidation reactions of 1- and 2-naphthols: an experimental and theoretical study«. The Journal of Physical Chemistry A. Zv. 117, št. 44. 7. november 2013. str. 11261–70. Bibcode:2013JPCA..11711261S. doi:10.1021/jp4081355. PMID 24093754. Pridobljeno 2. decembra 2013.
- ↑ Isaksen, I.S.A.; S.B. Dalsøren (2011). »Getting a better estimate of an atmospheric radical«. Science. 331 (6013): 38–39. Bibcode:2011Sci...331...38I. doi:10.1126/science.1199773. PMID 21212344. Pridobljeno 9. januarja 2011.
- ↑ Heal MR, Heard DE, Pilling MJ, Whitaker BJ (1995). »On the development and validation of FAGE for local measurement of tropospheric OH and HO2«. Journal of Atmospheric Sciences. 52 (19): 3428–3448. Bibcode:1995JAtS...52.3428H. doi:10.1175/1520-0469(1995)052<3428:OTDAVO>2.0.CO;2. ISSN 1520-0469.
- ↑ Montzka, S.A.; M. Krol; E. Dlugokencky; B. Hall; P. Jöckel; J. Lelieveld (2011). »Small interannual variability of global atmospheric hydroxyl«. Science. 331 (6013): 67–69. Bibcode:2011Sci...331...67M. doi:10.1126/science.1197640. PMID 21212353. Pridobljeno 9. januarja 2011.
- ↑ Reinke-Kunze, Christine (1994). Alfred Wegener. Basel: Birkhäuser Basel. str. 153–157. doi:10.1007/978-3-0348-6343-8_14. ISBN 9783034863445.
