Anilin
| |||
| Imena | |||
|---|---|---|---|
| IUPAC ime
fenilamin
| |||
| Druga imena
fenilamin,
aminobenzen, benzenamin | |||
| Identifikatorji | |||
3D model (JSmol)
|
|||
| ChemSpider | |||
| ECHA InfoCard | 100.000.491 | ||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Lastnosti | |||
| C6H7N | |||
| Molska masa | 93,13 g·mol−1 | ||
| Videz | brezbarvna tekočina | ||
| Gostota | 1.021,7 kg/m3, tekoč | ||
| Tališče | -6,3 °C | ||
| Vrelišče | 184,13 °C | ||
| 3,6 g/100 mL pri 20 °C | |||
| Kislost (pKa) | približno 27 | ||
| Bazičnost (pKb) | 9,42 | ||
| Viskoznost | 3,71 mPa·s pri 25 °C | ||
| Termokemija | |||
Std sežigna
entalpija (ΔcH⦵298) |
-3394 kJ/mol | ||
| Nevarnosti | |||
EU klasifikacija (DSD) (zastarelo)
|
Karcinogen (kategorija 3) Mutagen (kategorija 3) | ||
| R-stavki (zastarelo) | R23/24/25, R40, R41, R43, Predloga:R48/23/24/25, Predloga:R68, R50 | ||
| S-stavki (zastarelo) | (S1/2), S26, Predloga:S27, S36/37/39, (S45), Predloga:S46, (S61), Predloga:S63 | ||
| NFPA 704 (diamant ognja) | |||
| Sorodne snovi | |||
| Sorodne snovi | fenilhidrazin, nitrozobenzen, nitrobenzen | ||
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |||
| Sklici infopolja | |||
Anilin, fenilamin ali aminobenzen je organska spojina s kemijsko formulo C6H5NH2. Anilin je najenostavnejši in eden od najpomembnejših aromatskih aminov. Anilin je brezbarvna oljnata tekočina pekočega aromatičnega okusa z neprijetnim vonjem po pokvarjenih ribah. Je zelo toksičen, lahko vnetljiv in gori s sajastim plamenom. Največ anilina se porabi za sintezo bolj kompleksnih organskih spojin, na primer poliuretanov in barvil.
Zgodovina
[uredi | uredi kodo]Anilin je prvi izoliral Otto Unverdorben[1] leta 1826 z destruktivno destilacijo indiga in ga imenoval kristalin. Leta 1834 je Friedrich Runge iz premogovega katrana izoliral neznano snov, ki je se je po obdelavi s klorovim apnom modro obarvala. Imenoval jo je kianol (ali cianol). Leta 1841 je Carl Julius Fritzsche pri obdelavi indiga s kalijevim hidroksidom pridobil oljnato snov in jo po eni od rastlin, iz katere se pridobiva indigo (indigofera anil), imenoval anilin. Približno istočasno je Nikolaj Nikolajevič Zinin pridobil anilin z redukcijo nitrobenzena in ga imenoval benzidam. Leta 1855 je vse te produkte raziskal August Wilhelm von Hofmann in ugotovil, da gre za isto snov in jo imenoval anilin oziroma fenilamin.
Industrijska predelava anilina se je začela v poznih 1850. in 1860. letih s proizvodnjo prvega sintetičnega barvila moveina, imenovanega tudi anilinski purpur, ki ga je leta 1856 odkril Hofmannov študent William Henry Perkin. Anilin je bil v času odkritja moveina draga laboratorijska kemikalija, kmalu zatem pa se je začel proizvajati industrijsko po postopku, ki ga je odkril Antoine Béchamp.[2] Industrijska proizvodnja anilina je povzročila hiter razvoj industrije sintetskih barvil.
Sinteza
[uredi | uredi kodo]Industrijska sinteza anilina poteka v dveh korakih: prvi korak je nitriranje benzena, kateremu sledi redukcija (hidrogeniranje) nitrobenzena v anilin:
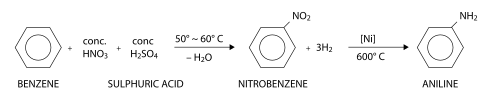
Benzen se nitrira z zmesjo koncentrirane dušikove kisline (HNO3) in žveplove kisline (H2SO4) pri temperaturi 50-60 °C, pri čemer nastane nitrobenzen. Drugi korak je hidrogeniranje nitrobenzena v anilin pri približno 600 °C v prisotnosti niklja kot katalizatorja. Laboratorijsko hidrogeniranje nitrobenzena poteka z vodikom, ki nastaja sproti v reakcijski zmesi iz železovih opilkov in klorovodikove kisline.
Anilin se lahko sintetizira tudi iz fenola in amonijaka.
Derivati anilina
[uredi | uredi kodo]Mnogo derivatov anilina se lahko pripravi na podoben način kot anilin.
Tehnični anilin se trži kot "anilinsko olje za modro", ki je čisti anilin, "anilinsko olje za rdeče", ki je ekvimolarna zmes anilina ter orto- in para-toluidina in "anilinsko olje za safranin", ki vsebuje anilin in orto-toluidin in se pridobiva z destilacijo taline fuksina.
Kemijske lastnosti
[uredi | uredi kodo]Oksidacija
[uredi | uredi kodo]Anilin je pri normalnih pogojih brezbarvna oljnata tekočina, ki na zraku počasi oksidira in se zasmoli. Barva prehaja iz brezbarvne v rumeno in nato v rdečerjavo barvo. Oksidacija anilina je dobro raziskana. V alkalnih raztopinah nastaja azobenzen, v prisotnosti arzenove kisline pa vijolično obarvani violanin. Kromova kislina pretvori anilin v kinon. Z oksidacijo s klorati v prisotnosti nekaterih (predvsem vanadijevih) kovinskih soli nastane barvilo anilinsko črno. Klorovodikova kislina in kalijev klorat dajeta kloranil. Kalijev permanganat v nevtralnem mediju oksidira anilin v nitrobenzen, v alkalnem mediju pa v azobenzen. Amonijak in oksalna kislina v kislih raztopinah oskidirata anilin v anilinsko črno. V reakciji s hipoklorovo kislino nastajata 4-aminofenol in para-amino difenilamin.
Bazičnost
[uredi | uredi kodo]Anilin je rahlo bazičen. Aromatski amini so na splošno mnogo šibkejše baze kot alifatski amini. Anilin tvori z močnimi kislinami anilinijev (ali fenilamonijev) ion C6H5-NH3+. Anilin kljub temu, da je šibka baza, obarja cinkove, aluminijeve in železove soli in izganja amonijak iz njegovih soli. Šibka bazičnost je posledica negativnega induktivnega efekta, ker je samski eletronski par dušika delno delokaliziran v π sistem benzenovega obroča.
Aciliranje
[uredi | uredi kodo]Anilin reagira s karboksilnimi kislinami,[3] še raje pa z njihovimi anhidridi in tvori amide, ki se včasih imenujejo tudi anilidi: spojina CH3-CO-NH-C6H5, ki nastane iz ocetne kisline in anilina, je acetanilid. Njeno komercialno ime je antifebrin in se uporablja kot antipiretik in analgetik.
N-alkil derivati
[uredi | uredi kodo]Anilin se spaja z alkil jodidi in tvori sekundarne in terciarna amine. Metil in dimetil anilin sta brezbarvni tekočini, ki se pripravljata s segrevanjem anilina, anilin hidroklorida in metanola v avtoklavu pri 220 °C. Obe spojini sta pomembni surovini za sintezo barvil. Metil anilin ima vrelišče 193-195 °C, dimetil anilin pa 192 °C.
Žveplovi derivati
[uredi | uredi kodo]Pri kuhanju anilina z ogljikovim disulfidom nastaja sulfokarbanilid (difenil tiosečnina) CS(NHC6H5)2, ki lahko razpade v fenil izotiocianat (C6H5CNS) in trifenil guanidin (C6H5N=C(NHC6H5)2).
Anilin se obnaša podobno kot fenol in je zelo dovzeten za elektrofilne substitucije. V reakciji z žveplovo kislino pri 180 °C nastane sulfanilna kislina (NH2C6H4SO3H), katero se lahko pretvori v sulfanilamid. Sulfanilamid je eno zdravil, ki se je v 20. stoletju uporabljalo kot baktericid.
Diazotiranje
[uredi | uredi kodo]Anilin in njegovi derivati s subtituiranim obročem reagirajo z dušikasto kislino (HNO2) in tvorijo diazonijeve soli. Anilinova –NH2 skupina se preko diazonijevih lahko pretvori v –OH, -CN ali halogenid (Sandmeyerjeve reakcije).
Druge reakcije
[uredi | uredi kodo]Anilin reagira z nitrobenzenom in tvori fenazin (Wohl-Auejeva reakcija).
Acetanilid se uporablja v anilin acetatnem testu ogljikovih hidratov za identificiranje pentoz, ki jih pretvori v furfural.
Uporaba
[uredi | uredi kodo]
Leta 1856 je William Henry Perkin iz anilina sintetiziral prvo umetno barvilo movein oziroma anilinski purpur. Moveinu je sledila široka paleta drugih barvil, med katerimi so bili najpomebnejša fuksin, safranin in indulin in anilin je dobil zelo visoko tehnološko in tržno vrednost. Barvilom so sledila zdravila, na primer antipiretik in analgetik paracetamol (N-(4-hidroksifenil)etanamid) s komercialnim imenom Tylenol.
Anilin se v biologiji uporablja za barvanje nervne RNK (Nisslovo barvanje). RNK se obarva modro, kar omogoča selektivno vizualizacijo nevronskih celičnih teles.
V sodobnem času se okrog 85% svetovne proizvodnje anilina porabi za sintezo metilen difenil diizocianata (MDI), ki je surovina za poliuretane, 9% za pomožna sredstva v gumarski industriji, 2% za herbicide in samo 2% za barvila in pigmente.[4]
Polimerizirani anilin se uporablja kot polprevodniški elektrodni most, na primer v biosenzorjih.
Toksičnost
[uredi | uredi kodo]Anilin je toksičen. Do zastrupitve z njm lahko pride z vdihavanjem hlapov, zaužitjem ali resorbcijo skozi kožo. Povzroča glavobol, zaspanost, cianozo in duševno zmedenost, pri težjih zastrupitvah tudi krče. Daljša izpostavljenost param ali izpostavljenost kože vpliva na živčni sistem in krvni obtok in povzroči utrujenost, izgubo apetita, glavobol in vrtoglavico.[5]
Spomladi in poleti 1981 se je v Španiji 20.000 prebivalcev zastrupilo z repičnim oljem, ki je bilo denaturirano z anilinom. 12.000 ljudi so morali hospitalizitrati, več kot 350 ljudi pa je umrlo. Natančni vzroki zastrupitve če vedno niso znani.
Nekateri strokovnjaki uvrščajo anilim med karcinogene snovi, čeprav ga IARC (Mednarodna agencija za raziskavo raka) uvršča v 3. kategorijo med "snovi, ki se jih ne da uvrstiti med povzročitelje raka pri človeku". Takšna razvrstitev je posledica omejenih in nasprotujočih si podatkov o njegovi toksičnosti.
Reference
[uredi | uredi kodo]- ↑ Otto Unverdorben (1826). »Ueber das Verhalten der organischen Körper in höheren Temperaturen«. Annalen der Physik. 84 (11): 397–410. doi:10.1002/andp.18260841109.
- ↑ Perkin, William Henry. 1861-06-08. "Proceedings of Checmical Societies: Chemical Society, Thursday, May 16, 1861." The Chemical News and Journal of Industrial Science. Pridobljeno 2007-09-24.
- ↑ C.N. Webb: Benzanilide, Org. Synth., Vol. 1 (1941), str. 82
- ↑ »Aniline«. The Chemical Market Reporter. Pridobljeno 21. decembra 2007.
- ↑ Muir, GD (ed.) 1971, Hazards in the Chemical Laboratory, The Royal Institute of Chemistry, London.



