Grignardova reakcija
Grignardova reakcija je organokovinska kemijska reakcija, v kateri alkilni ali arilni magnezijevi halogenidi (Grignardovi reagenti) delujejo kot nukleofili in napadejo elektrofilne ogljikove atome v polarnih kemijskih skupinah, na primer v karbonilni skupini. Hibridizacija orbital okrog reakcijskega centra se zato spremeni in v reakciji nastane nova vez ogljik-ogljik.[1] Grignardova reakcija je zato zelo pomembno orodje za formiranje novih vezi ogljik-ogljik,[2][3] pa tudi za formiranje vezi ogljik-fosfor, ogljik-kositer, ogljik-silicij, ogljik-bor in ogljik-heteroatom.
Reakcija je dobila ime po francoskemu kemiku in Nobelovemu nagrajencu Victorju Grignardu.
Grignardovo reakcijo v splošni obliki se lahko zapiše z naslednjo kemijsko enačbo:

Adicija na nukleofil je zaradi visoke vrednosti pKa alkilne komponente ireverzibilna (pKa≈45). Grignardov reagent s splošno formulo R-MgBr ali Ar-MgBr reagira z elektrofilnimi kemijskimi spojinami. Reakcije niso ionske. Njegova pomanjkljivost je, da zelo hitro reagira s protičnimi topili, na primer z vodo, ali funkcionalnimi skupinami s kislimi protoni, na primer z alkoholi in amini. V laboratoriju lahko na potek reakcije vpliva celo zračna vlaga, zato se reakcijsko posodo pred reakcijo običajno temeljito posuši s plamenom plinskega gorilnika in zapre, da se prepreči kasnejši vdor vlage.
V industrijskem merilu je Grignardova reakcija ključni korak na primer v sintezi zdravila Tamoksifen,[4] ki se uporablja za zravljenje raka dojke:
Reakcijski mehanizem[uredi | uredi kodo]
Adicija Grignardovega reagenta na karbonil poteka običajno preko prehodne spojine s šestčlenskim obročem:[5]

V sterično oviranih Grignardovih reagentih se reakcija lahko nadaljuje s prenosom enega samega elektrona.
V reakcijah z Grignardovmi reagenti ne sme biti prisotna voda, ki povzroči hiter razpad reagenta. Večina reakcij zato poteka v brezvodnih topilih, na primer dietil etru ali tetrahidrofuranu (THF), ker kisikov atom v teh topilih stabilizira Grignardov reagent. Reagent lahko reagira tudi s kisikom iz zraka, tako da se kisikov atom vrine med ogljikovo osnovo in magnezijevo halogenidno skupino. Nezaželene stranske reakcije se lahko v veliki meri omeji tako, da se s parami hlapnega topila izpodrine zrak nad reakcijsko zmesjo. Še bolje je, da reakcija poteka v inertni atmosferi dušika ali argona.
Sinteza Grignardovih reagentov[uredi | uredi kodo]

Grignardovi reagenti so spojine, ki nastajajo v reakcijah med alkilnimi ali arilnimi halogenidi in kovinskim magnezijem.[6] Reakcija poteka tako, da se v suspenzijo magnezija v dietil etru ali tetrahidrofuranu dodaja organski halogenid. Topilo prispeva ligande, ki so potrebni za stabilizacijo organomagnezijeve spojine. Kisik in protična topila, na primer voda i alkoholi, niso zaželeni, ker reagirajo z Grignardovimi reagenti.
Začetek reakcije je po navadi počasen, ker poteka na fazni meji med trdno snovjo in raztopino. Iniciaciji reakcije sledi obdobje indukcije, v katerem začne aktivirani magnezij reagirati z organskimi reagenti. Po indukciji postane reakcija zelo eksotemna. Najpogostejši organski reagenti so alkilni in arilni bromidi in jodidi. Uporabni so tudi kloridi, fluoridi pa so nereaktivni. Reagirajo samo s posebno aktiviranim magnezijem, na primer z Riekejevim magnezijem.
Nekateri Grignardovi reagenti, na primer metilmagnezijev klorid, fenilmagnezijev bromid in alilmagnezijev bromid, so komercialni produkti, raztopljeni v tetrahidrofuranu ali dietil etru.
Mnogi Grignardovi reagenti tvorijo zaradi Schlenkovega ravnotežja različno količino diorganomagnezijevih spojin:
- 2RMgX ↔ R2Mg + MgX2
Iniciacija[uredi | uredi kodo]
Površina kovinskega magnezija je običajno prevlečena s pasivnim slojem magnezijevega oksida (MgO), ki ga je treba odstraniti, da pride kovina v stik z zelo reaktivnim organskim halogenidom.
Za iniciranje Grignardove reakcije je več metod. Med mehanske metode spadajo drobljenje magnezija v sami reakcijski zmesi, ki poveča njegovo površino, intenzivno mešanje in uporaba ultrazvoka. Med kemijske metode spada aktiviranje magnezija z jodom, metil jodidom ali 1,2-dibromoetanom. Posebno uporaben je 1,2-dibromoetan, katerega delovanje se lahko opazuje z nastajanjem mehurčkov etena in daje neškodljive stranske produkte:
- Mg + BrC2H4Br → C2H4 + MgBr2
Ugodno delujejo tudi majhne količine živosrebrovega(II) klorida, ki amalgamira površino magnezija in poveča njegovo reaktivnost. Poraba magnezija za iniciacijo reakcije je neznatna.
Reakcije[uredi | uredi kodo]
Reakcije s karbonili[uredi | uredi kodo]
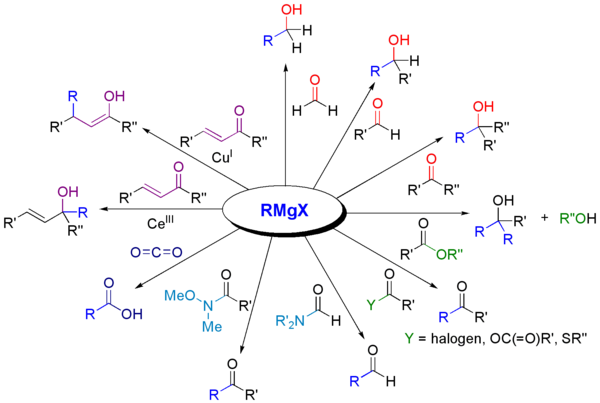
Reakcije z elektrofili[uredi | uredi kodo]

Tvorba vezi s heteroatomi[uredi | uredi kodo]

Pripajanje[uredi | uredi kodo]
Grignardov reagent je lahko vključen tudi v reakcije pripajanja. Primer: nonilmagnezijev bromid v prisotnosti železovega(III) acetilacetonata reagira z aril kloridom, tako da nastane nonilbenzojeva kislina:[7]

Dobri katalizatorji za pripajanje aril halogenidov na arilne Grignardove reagente je nikljev(II) klorid v tetrahidrofuranu (THF). Učinkovit katalizator za pripajanje alkil halogenidov je dilitijev tetrahidrokuprat (Li2CuCl4), pripravljen z mešanjem litijevega klorida (LiCl) in bakrovega(II) klorida (CuCl2) v THF. Pripajanje Kumada-Corriu omogoča sintezo stirenovih derivatov.
Oksidacija[uredi | uredi kodo]
Oksidacija Grignardovega reagenta s kisikom poteče preko radikalskega vmesnega produkta v magnezijev hidroperoksid. S hidrolizo nastalega kompleksa nastane hidroperoksid, z redukcijo z dodatnim ekvivalentom Grignardovega reagenta pa alkohol.
Če je pri oksidaciji Grignardovega reagenta s kisikom prisoten alken, nastane za etilen podaljšan alkohol.[8]

Takšna modificirana oksidacija poteče samo z arilnimi ali vinilnimi Grignardovimi reagenti. V reakciji mora biti prisoten kisik, ker brez njega reakcija ne poteče. Edina slabost reakcije je, da zahteva najmanj dva ekvivalenta Grignardovega reagenta. Slabost se lahko delno obide z uporabo dvojnega Grignardovega sistema s cenenimi reagenti, na primer z n-butilmagnezijevim bromidom.
Nukleofilna alifatska substitucija[uredi | uredi kodo]
V nukleofilnih alifatskih substitucijah, na primer z alkil halogenidi, imajo Grignardovi reagenti vlogo nukleofila. Takšna substitucija je ključna reakcija pri industrijski sintezi nesteroidnega protivnetnega zdravila Naproxena:

Eliminacija[uredi | uredi kodo]
V Boordovi sintezi alkenov (olefinov) sproži dodatek magnezija k nekaterim β-halogenetrom eliminacijo halogena in skupine RO- in tvorbo alkena. Eliminacija je v nekaterih primerih nezaželena, ker omeji uporabnost Grignardovih reakcij.

Grignardova degradacija[uredi | uredi kodo]
Grignardova degradacija[9][10] je reakcija, ki se je nekoč uporabljala za ugotavljanje sestave spojin. V reakciji heteroaril bromida (HetBr) z magnezijem nastane Grignardov reagent RMgBr, ki reagira z vodo v HetH (brom se substituira z vodikom). Hidroliza omogoča ugotavljanje števila atomov halogena v organski spojini. Grignardova degradacija se v sodobni organski analizni kemiji uporablja za analiziranje nekaterih triacilglicerolov.[11]
Galerija[uredi | uredi kodo]
-
V reakcijsko posodo se vsujejo lističi kovinskega magnezija.
-
Nanje se nalije tetrahidrofuran. Reakcijski zmesi se doda majhen košček joda.
-
Zmesi se med segravanjem doda raztopina alkil bromida.
-
Ko je dodajanje končano, se zmes še nekaj časa segreva.
-
Tvorba Grignardovega reagenta je končana. V reakcijski posodi je ostalo še nekaj nezreagiranega magnezija.
-
Grignardov reagent se pred dodatkom karbonilne spojine ohladi na 0 °C. Raztopina postane motna, ker se del Grignardovega reagenta izloči.
-
Raztopini Grignardovega reagenta se doda karbonilna spojina.
-
Raztopina se segreje na sobno temperaturo. Reakcija je zaključena.
Reference[uredi | uredi kodo]
- ↑ Grignard, V. (1900), »Sur quelques nouvelles combinaisons organométaliques du magnésium et leur application à des synthèses d'alcools et d'hydrocabures«, Compt. Rend., 130: 1322–1325
- ↑ Shirley, D. A. (1954), »The Synthesis of Ketones from Acid Halides and Organometallic Compounds of Magnesium, Zinc, and Cadmium«, Org. React, 8: 28–58
- ↑ Huryn, D. M. (1991), »Carbanions of Alkaki and Alkaline Earth Cations:(ii) Selectivity of Carbonyl Addition Reaction«, Comp. Org. Syn, 1: 49–75
- ↑ »Grignard Reagents: New Developments«, ISBN: 0–471
- ↑ Maruyama, K.; Katagiri, T. (1989), »Mechanism of the Grignard reaction«, J. Phys. Org. Chem, 2: 205, doi:10.1002/poc.610020303
- ↑ Lai Yee Hing (1981), »Grignard Reagents from Chemically Activated Magnesium«, Synthesis, 1981: 585–604, doi:10.1055/s-1981-29537
- ↑ A. Fürstner, A. Leitner, G. Seidel (2004). »4-Nonylbenzoic Acid«. Org. Synth. 81: 33-42.
- ↑ Nobe, Youhei; Arayama, Kyohei; Urabe, Hirokazu (2005), »Air-Assisted Addition of Grignard Reagents to Olefins. A Simple Protocol for a Three-Component Coupling Process Yielding Alcohols«, J. Am. Chem. Soc., 127 (51): 18006–18007, doi:10.1021/ja055732b
- ↑ Steinkopf, Wilhelm (1934), »Studien in der Thiophenreihe. XXVI. Isomere Bromthiophene und die Konstitution der Thiophendisulfonsäuren«, Justus Liebig s Annalen der Chemie, 512: 136, doi:10.1002/jlac.19345120113
- ↑ Steinkopf, Wilhelm (1940), »Studien in der Thiophenreihe. LI. Atophanartige Derivate des Dithienyls und Diphenyls«, Justus Liebig s Annalen der Chemie, 543: 119, doi:10.1002/jlac.19405430110
- ↑ Myher JJ; Kuksis A (Februar 1979), »Stereospecific analysis of triacylglycerols via racemic phosphatidylcholines and phospholipase C«, Can. J. Biochem., 57 (2): 117–24, PMID 455112










