Svinčev(II) oksid

| |
| |
| Imena | |
|---|---|
| IUPAC ime
svinčev(II) oksid
| |
| Druga imena
svinčev monoksid
svinčev oksid | |
| Identifikatorji | |
| ECHA InfoCard | 100.013.880 |
PubChem CID
|
|
| RTECS število |
|
| UN število | 3288 |
CompTox Dashboard (EPA)
|
|
| Lastnosti | |
| PbO | |
| Molska masa | 223,20 g/mol |
| Videz | rdeč ali rumen prah |
| Gostota | 9,53 g/cm3 |
| Tališče | 888 °C (1.630 °F; 1.161 K) |
| Vrelišče | 1.477 °C (2.691 °F; 1.750 K) |
| 0,00504 g/100 mL (α-oblika) 0,01065 g/100 mL (β-oblika) | |
| Topnost | netopen v razredčenih alkalijah in etanolu, topen v koncentriranih alkalijah, koncentrirani klorovodikovi kislini in amonijevem kloridu |
| Struktura | |
| Kristalna struktura | tetragonalna, Pearsonov symbol tP4 |
| Prostorska skupina | P4/nmm, No. 129 |
| Nevarnosti | |
EU klasifikacija (DSD) (zastarelo)
|
• Repr. Cat. 1/3 |
| R-stavki (zastarelo) | R61, R20/22, R33, R62, R50/53 |
| S-stavki (zastarelo) | S53, (S45), S60, (S61) |
| NFPA 704 (diamant ognja) | |
| Plamenišče | ni vnetljiv |
| Sorodne snovi | |
| Drugi anioni | svinčev sulfid svinčev selenid svinčev telurid |
| Drugi kationi | ogljikov monoksid silicijev monoksid kositrov(II) oksid |
| Sorodno svinčevi oksidi | svinčev(II,II,IV) oksid svinčev dioksid |
| Sorodne snovi | talijev(III) oksid bizmutov(III) oksid |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Svinčev(II) oksid, svinčev oksid ali svinčev monoksid je anorganska spojina s formulo PbO. Spojina ima dva polimorfa: tetragonalni litargit in ortorombski masikot.
Največ svinčevega oksida se porabi za proizvodnjo svinčevih stekel in industrijske keramike, vključno z računalniškimi komponentami.
Priprava[uredi | uredi kodo]
PbO se lahko pripravi s segrevanjem kovinskega svinca pri približno 600 °C. Pri tej temperaturi je PbO končni produkt oksidacije svinca v različne okside:[1]
- do 293 °C: PbO2 → 293 °C: Pb12O19 → 351 °C: Pb12O17 → 375 °C: Pb3O4 → 605 °C: PbO
Pripravi se lahko tudi z razpadom svinčevega(II) nitrata in svinčevega(II) karbonata:
- 2Pb(NO3)2 → 2PbO + 4NO2 + O2
- PbCO3 → PbO + CO2
V industrijskem obsegu se proizvaja kot vmesni produkt predelave svinčeve rude v kovinski svinec. Svinčev sulfid (galenit) se pri praženju pri visoki temperaturi (1000 °C) pretvorijo v oksid:[2]
- 2PbS + 3O2 → 2PbO + 2SO2
Kovinski svinec se pridobiva z redukcijo PbO z ogljikovim monoksidom pri približno 1200 °C:[3]
- PbO + CO → Pb + CO2
Zgradba[uredi | uredi kodo]
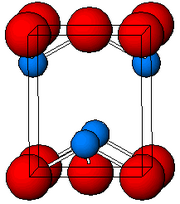
Z rentgensko kristalografijo se je ugotovilo, da imata oba polimorfa, tetragonalni in ortorombski, obliko piramide s štirikratno koordiniranimi Pb centri. Tetragonalni PbO ima štiri enako dolge vezi Pb-O, ortogonalni pa dve krajši in dve daljši vezi. Piramidasta oblika kaže na prisotnost stereokemijsko aktivnega prostega elektronskega para.[4] Tetragonalni PbO se imenuje litargit, ortorombski pa masikot. Prehod masikota v litargit in obratno se doseže z nadzorovanim segrevanjem oziroma ohlajanjem.[5][6] Tetragonalna oblika je običajno rdeče ali oranžne barve, vendar barva ni najbolj zanesljiv pokazatelj njegove zgradbe.[7] Mineralni obliki obeh polimorfov sta v naravi redki.
Reakcije[uredi | uredi kodo]
Rdeča in rumena različica PbO se razlikujeta samo po majhni spremembi entalpije:
- PbO(rdeč) → PbO(rumen); ΔH = 1,6 kJ/mol
PbO je amfoteren, se pravi da reagira s kislinami in bazami. S kislinami tvori Pb2+ soli, ki nastanejo preko klastrov, na primer [Pb6O(OH)6]4+. Z močnimi bazami tvori soli plumbite:[8]
- PbO + H2O + OH- → [Pb(OH)3]-
Uporaba[uredi | uredi kodo]
PbO je ključna surovina za proizvodnjo svinčevega stekla. Svinčev oksid zmanjša viskoznost steklene taline, v steklu pa poveča njegov lomni količnik, električno upornost in sposobnost absorbiranja rentgenskih žarkov. Kot dodatek v industrijsko keramiko (in steklo) poveča njegovo magnetnost (dvigne Curiejevo temperaturo).[9] V preteklosti se je na veliko uporabljal tudi za keramične glazure za kuhinjsko posodo. Njegova uporaba v ta namen je sedaj mnogo manjša. Nekaj PbO se porabi tudi za vulkanizacijo gume, pigmente in barvne premaze.[10] V katodnih ceveh se uporablja za blokiranje rentgenskega sevanja, predvsem v vratu in lijaku, ker na čelni ploskvi lahko povzroči razbarvanje. Za čelno ploskev je bolj primeren stroncijev oksid.
Proizvodnja svinca, torej tudi svinčevega oksida, je odvisna od števila avtomobilov, ker je svinec ključna komponenta avtomobilskih svinčevih akumulatorjev.[11]
Drugo[uredi | uredi kodo]
Zmes PbO in glicerina se strdi v trden vodoodporen cement, ki se je včasih uporabljal za tesnenje stranic in dna akvarijev in stekla v okenskih okvirih.
Litargit se je včasih mešal z lanenim oljem in kuhal, da je nastal vodoodporen premaz, ki so ga uporabljali za pozlačevanje. Laneno olje je dalo premazu oprijemljivost in odpornost, litargit pa temno rdečo barvo, tako da so bili zlati lističi videti topli in sijoči.
PbO se uporablja v nekaterih kondenzacijskih reakcijah v organskih sintezah.[12]
Alkimija[uredi | uredi kodo]
Svinčev oksid je igral pomembno vlogo v alkimiji. Svinec se je v kemijski reakciji pretvoril v rumen PbO, za katerega so verjeli, da je zlato. Reakcijo so imeli za dokaz, da lahko zlato nastane tudi iz neplemenite kovine.
Vpliv na zdravje[uredi | uredi kodo]
Vdihavanje in zaužitje svinčevega oksida je smrtno nevarno. PbO povzroča draženje kože, oči in dihal, vpliva na dlesni, osrednje živčevje, ledvica in reproduktivni sistem in se akumulira v tkivih rastlin in sesalcev.[13]
Sklici[uredi | uredi kodo]
- ↑ N.N. Greenwood, A. Earnshaw (1997). Chemistry of Elements. 2. izdaja. Butterworth-Heinemann.
- ↑ A.M. Abdel-Rehim (2006). Thermal and XRD analysis of Egyptian galena. Journal of Thermal Analysis and Calorimetry 86 (2): 393–401.
- ↑ Lead Processing. Universalium.academic.ru.
- ↑ A.F. Wells (1984). Structural Inorganic Chemistry (5 izd.). Oxford: Clarendon Press. COBISS 621359. ISBN 0-19-855370-6.
- ↑ A. De Kumar (2007). A Text Book of Inorganic Chemistry. str. 383.
- ↑ The Chemistry of Metal Alkoxides. Kluwer Academic Publishers (2002), odstavek 9.4, str. 115.
- ↑ D.J. Rowe (1983). Lead manufacturing in Britain. Str. 16.
- ↑ Holleman, A. F.; in sod. (2001). Inorganic Chemistry (1 izd.). San Diego [etc.] : Academic Press ; Berlin ; New York : De Gruyter, cop. COBISS 24318981. ISBN 0-12-352651-5.
- ↑ Ceramic and Glass Materials: Structure, Properties and Processing. 9. poglavje: Lead Compounds. Springer (2008).
- ↑ D.S. Carr (2002). Lead Compounds. Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinhiem. doi: 10.1002/14356007.a15_249.
- ↑ C.A. Sutherland, E.F. Milner, R.C. Kerby, H. Teindl, A. Melin, H.M. Bolt (2005). Lead. Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim. doi: 10.1002/14356007.a15_193.pub2.
- ↑ B.B. Corson (1936). 1,4-Diphenylbutadiene. Org. Synth. 16: 28, 2: 229.
- ↑ Lead (II) oxide. International Occupational Safety and Health Information Centre. Pridobljeno 6. junija 2009.

