Cinkov klorid: Razlika med redakcijama
Brez povzetka urejanja |
Brez povzetka urejanja |
||
| Vrstica 1: | Vrstica 1: | ||
{{v delu}} |
|||
'''Cinkov klorid''' je [[sol (kemija)|sol]] z molekulsko formulo [[cink|Zn]][[klor|Cl]]<sub>2</sub>. Pojavlja se kot beli higroskopni [[kristal]]i, ki lahko [[sublimacija|sublimirajo]]. |
'''Cinkov klorid''' je [[sol (kemija)|sol]] z molekulsko formulo [[cink|Zn]][[klor|Cl]]<sub>2</sub>. Pojavlja se kot beli higroskopni [[kristal]]i, ki lahko [[sublimacija|sublimirajo]]. |
||
Redakcija: 00:01, 14. maj 2013
Cinkov klorid je sol z molekulsko formulo ZnCl2. Pojavlja se kot beli higroskopni kristali, ki lahko sublimirajo.
Cinkov klorid uporabljajo kot katalizator, za konzerviranje lesa, v industriji barvil in kot talilo pri cinkanju. Je negorljiva snov.
Stik z cinkom in njegovimi raztopinami povzroča hude poškodbe/izjede kože, sluznice in oči. Nevarnost zastrupitve črevesja, ledvic in srca zaradi resorpcije skozi poškodovana mesta.
Predloga:Chembox Other
| |

| |
| Imena | |
|---|---|
| IUPAC ime
Cinkov klorid
| |
| Druga imena
Cink(II) klorid
Cink diklorid Cinkovo maslo | |
| Identifikatorji | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.028.720 |
| EC število |
|
PubChem CID
|
|
| RTECS število |
|
| UNII | |
| UN število | 2331 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Lastnosti | |
| ZnCl2 | |
| Molska masa | 136.315 g/mol |
| Videz | beli kristali hygroscopic |
| Vonj | brez vonja |
| Gostota | 2.907 g/cm3 |
| Tališče | 292 °C (558 °F; 565 K) |
| Vrelišče | 756 °C (1.393 °F; 1.029 K) |
| 4320 g/L (25 °C) | |
| Topnost | topljivo v etanolu, glicerolu in acetonu |
| Topnost (alkohol) | 4300 g/L |
| Struktura | |
| Koordinacijska geometrija |
Tetrahedral, linearno v plinasti fazi |
| Nevarnosti | |
EU klasifikacija (DSD) (zastarelo)
|
Harmful (Xn) Corrosive (C) Nevarno za okolje (N) |
| R-stavki (zastarelo) | R22, R34, R50/53 |
| S-stavki (zastarelo) | (S1/2), S26, S36/37/39, (S45), S60, (S61) |
| NFPA 704 (diamant ognja) | |
| Smrtni odmerek ali koncentracija (LD, LC): | |
LD50 (srednji odmerek)
|
350 mg/kg, rat (oral) |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Struktura in lastnosti
Znane so štiri kristalne oblike(polimorfi) ZnCl2 : α, β, γ in δ, in v vsakem primeru so Zn2+ ioni tetraedično usklajeni s štirimi klorovimi ioni. [1]
| Oblika | Simetrija | Simbol | Skupina | Št | a (nm) | b (nm) | c (nm) | Z | ρ (g/cm3) |
|---|---|---|---|---|---|---|---|---|---|
| α | Tetragonalna | tI12 | I42d | 122 | 0.5398 | 0.5398 | 0.64223 | 4 | 3.00 |
| β | Tetragonalna | tP6 | P42/nmc | 137 | 0.3696 | 0.3696 | 1.071 | 2 | 3.09 |
| γ | Monoklinska | mP36 | P21c | 14 | 0.654 | 1.131 | 1.23328 | 12 | 2.98 |
| δ | Ortorombska | oP12 | Pna21 | 33 | 0.6125 | 0.6443 | 0.7693 | 4 | 2.98 |
Tu so a, b in c sta mrežne konstante, Z je število strukturnih enot na enoto celic in ρ je gostota izračunana iz strukturnih parametrov.[2][3][4] Ob izpostavljenosti atmosferi se čista suha ortorombska oblika (δ) hitro spreminja v eno od drugih oblik. Možna razlaga je, da OH− ioni, ki izvirajo iz absorbirane vode olajšajo preureditve.[1] [5]
Hitro ohlajanje stopljenega ZnCl2 nam da trdno amorfno steklo. Kovalenten značaj suhega materiala je indiciran z relativno nizkim tališčem 275 ° C. [6] Nadaljni dokaz za kovalentnost je visoka topnost diklorida v eteričnih topilh kjer se formirajo vezi s formulo ZnCl2L2, pri čemer je L = vez kot je O(C2H5)2. V plinski fazi so molekule ZnCl2 linearne z dolžino vezi 205 pm . [7] Stopljeni ZnCl2 ima visoko viskoznost pri točki tališča in nizko električno prevodnost, ki se zelo poveča z višanjem temperature.[7][8]
Hidrati
Poznanih je pet hidratov Cinkovega klorida ZnCl2(H2O)n, kjer je n = 1, 1.5, 2.5, 3 in 4.[9] Tetrahidrat ZnCl2(H2O)4 kristalizira iz vodne rastopine Cinkovega klorida.[9]
Priprava in čiščenje
Nehidriran ZnCl2 lahko pripravimo iz Cinka in Hidrogen klorida.
- Zn(s) + 2 HCl → ZnCl2 + H2(g)
Hidriraneoblike in vodne raztopine lahko zlahka pripravimo z obdelavo Zn s Klorovodikovo kislino. Cinkov oksid in Cinkov sulfid reagirajo z HCl:
V nasprotju z mnogimi drugimi elementi Cink v bistvu obstaja v samo eni obliki oksida, 2+ kar zelo poenostavi prečiščevanje klorida.
Komercialni vzorci Cinkovega klorida navadno vsebujejo vodo in produkte hidrolize kot nečistoče. Taki vzorci se lahko prečistijo z rekristalizacijo iz vročega dioksana. Brezvodni vzorci se lahko prečistijo s sublimacijo v toku plina Vodikovega klorida, ki ji sledi segrevanje sublimata na 400 °C v toku suhega dušika. Najenostavnejša metoda pa je obdelava Cinkovega klorida s Tionilkloridom.[10]>
Reakcije
Staljen anhidrid ZnCl2 pri 500–700 °C raztaplja Cink in pri hitrem ohlajanju taline se formira rumeno diamagnetno steklo, ki vsebuje Zn2+
2 ion.[9]
Znano je število soli ki vsebujejo tetraklorcinkov anion, ZnCl2−
4.[7] "Caultonov reagent," V2Cl3(thf)6Zn2Cl6 je primer ki vsebuje soli Zn2Cl2−
6.[11][12]
Spojina Cs3ZnCl5 vsebuje tetraedične ZnCl2−
4 in Cl− anione.[1] Za spojine ni značilno da vsebujejo ZnCl4−
6 ion.[1]
Medtem ko je Cinkov klorid zelo topen v vodi, pa na raztopine ne moremo gledati le kot na raztopljne Zn2+ ione in Cl− ione, prisotne so tudi vrste ZnClxH2O(4−x).[13][14][15] Vodne raztopine ZnCl2 so kisle: 6 M vodna raztopina ima pH 1.[9]
Kislost vodne raztopine ZnCl2 relativno gledano na raztopine drugih Zn2+ soli je zaradi oblikovanja tetraedičnih kloro vodnih sestavov kjer zmanjšanje koordinacijskega števila iz 6 na 4, še nadalje oslabi O-H vezi v vodnih molekulah raztopine.[16]
V alkalni raztopini v prisotnosti OH− iona, so prisotni razni cink hidroksikloridni anioni v raztopini, npr. ZnOH3Cl2−, ZnOH2Cl2−
2, ZnOHCl2−
3, in Zn5OH2Cl3·H2O (simonkolleite) usedline.[17]
Ko spuščamo mehurčke amoniaka skozi raztopino Cinkovega klorida se ne izloča hdroksid, ampak se tvorijo kompleksne mešanice amoniaka, Zn(NH3)4Cl2 · H2O in v koncentratu ZnCl2(NH3)2.[18]
Uporaba
Kot metalurško topilo
Cinkov klorid ima sposobnost da napada kovinske okside in tvori z njimi derivate s MZnOCl2. Ta reakcija je pomembna za uporabnost ZnCl2 kot topilo za spajkanje — raztaplja oksidirano površino kovine in jo tako očisti.[9] Topila s ZnCl2 kot aktivno sestavino včasih imenujemo "kositrne tekočine". Tipično je to topilo pripravljeno z raztapljanjem cinkove folije v razredčeni klorovodikovi kislini, dokler se preneha tvoriti vodik. Zaradi svoje korozivne narave, to topilo ni uporabno v primerih kjer mora na površini ostati nek sloj, kot na primer v elektroniki. Zaradi teh lastnosti se tudi uporablja v proizvodnji magnezijevih cementov za zobne plombe in kot aktivna sestavina v nekaterih ustnih vodah.
V organski sintezi
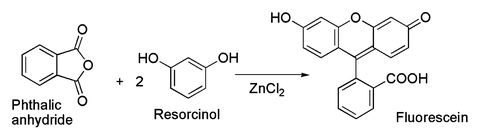
V laboratorijih je cinkov klorid široko uporaben v glavnem kot zmerno močna Lewisova kislina. Lahko je katalizator za Fischer indol sintezo,[19] kot tudi Friedel-Craftove acilacijske reakcije vklučujoč aktivirane aromatične obroče.[20][21]
V povezavi z zadnjim je to klasična priprava flurescenčnega barvila iz ftalanhidrida in resorcinola, ki vključuje Friedel-Craftovo acilacijo .[22] Ta transformacija je bila dejansko dosežena tudi z uporabo hidriranega ZnCl2 vzorec prikazan na zgornji sliki.
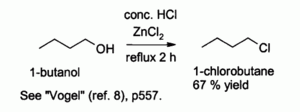
Sama klorovodikova kislina slabo eagira s primarnimi in sekundarnimi alkoholi, toda kombinacija HCl z ZnCl2 (poznana kot "Lucas reagent") je učinkovita za pripravo alkilnih kloridov. Tipične reakcije potekajo pri 130 ° C. Ta reakcija je verjetno poteka preko SN2 reakcijN2 mehanizma s primarnimi alkoholi ampak SN1 reakcijeN1 vodijo preko sekundarnih alkoholov.
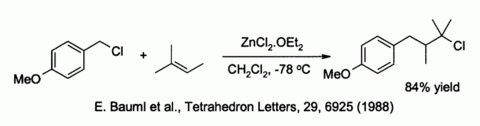
Cinkov klorid aktivira tudi benzilne in alilične halide v smeri zamenjave s šibkimi nukleofili kot so alkeni:[23]
Na podoben način, ZnCl 2 spodbuja selektivno NaBH 3 CN Znižanje terciarno, allylic ali benzil halide do ustreznih ogljikovodikov.
Cinkov klorid je tudi koristno začetni reagent za sintezo mnogih organozinc reagenti, kot so tiste, uporabljene v paladija katalizirane Negishi spenjanje s aril halogenidi s ali vinil halogenida s . [24] V takih primerih se organozinc spojina, ki ga transmetallation ponavadi pripravijo iz organolitijeva ali Grignardov reagent, na primer:
Cink enolat s, pripravljena iz alkalijskih enolates in ZnCl2, ki zagotavljajo nadzor nad stereokemija v aldolno kondenzacijski reakcije zaradi kelacije na cink. V prikazanem primeru spodaj treo produkt je imela prednost pred eritro s faktorjem 5:1, ko ZnCl2 v DME / eter je bil uporabljen [25] kelat je bolj stabilen, če je debeli fenilna skupina psevdo-ekvatorialni kot psevdo- aksialni, tj treo namesto eritro.
Za obdelavo tkanin
Za dimne bombe
Za odkrivanje prstnih odtisov
Kot razkužilo
Skrb za varnost
Reference
Zunanje povezave
Viri
- ↑ 1,0 1,1 1,2 1,3 Wells, A. F. (1984). Structural Inorganic Chemistry. Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ↑ Oswald, H. R.; Jaggi, H. (1960). »Zur Struktur der wasserfreien Zinkhalogenide I. Die wasserfreien Zinkchloride«. Helvetica Chimica Acta. 43 (1): 72–77. doi:10.1002/hlca.19600430109.
- ↑ Brynestad, J.; Yakel, H. L. (1978). »Preparation and Structure of Anhydrous Zinc Chloride«. Inorganic Chemistry. 17 (5): 1376–1377. doi:10.1021/ic50183a059.
- ↑ Brehler, B. (1961). »Kristallstrukturuntersuchungen an ZnCl2«. Zeitschrift für Kristallographie. 115 (5–6): 373–402. doi:10.1524/zkri.1961.115.5-6.373.
- ↑ Mackenzie, J. D.; Murphy, W. K. (1960). »Structure of Glass-Forming Halides. II. Liquid Zinc Chloride«. The Journal of Chemical Physics. 33 (2): 366–369. doi:10.1063/1.1731151.
{{navedi časopis}}: Vzdrževanje CS1: več imen: seznam avtorjev (povezava) - ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. izd.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ 7,0 7,1 7,2 Prince, R. H. (1994). King, R. B. (ur.). Encyclopedia of Inorganic Chemistry. John Wiley & Sons. ISBN 0-471-93620-0.
- ↑ Ray, H. S. (2006). Introduction to Melts: Molten Salts, Slags and Glasses. Allied Publishers. ISBN 81-7764-875-6.
- ↑ 9,0 9,1 9,2 9,3 9,4 Holleman, A. F.; Wiberg, E. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 0-12-352651-5.
{{navedi knjigo}}: Vzdrževanje CS1: več imen: seznam avtorjev (povezava) - ↑ Pray, A. P. (1990). Inorganic Syntheses. Zv. 28. New York: J. Wiley & Sons. str. 321–322. ISBN 0-471-52619-3. Describes the formation of anhydrous LiCl, CuCl2, ZnCl2, CdCl2, ThCl4, CrCl3, FeCl3, CoCl2, and NiCl2 from the corresponding hydrates.
- ↑ Mulzer, J.; Waldmann, H., ur. (1998). Organic Synthesis Highlights. Zv. 3. Wiley-VCH. ISBN 3-527-29500-3.
{{navedi knjigo}}: Vzdrževanje CS1: več imen: seznam urednikov (povezava) - ↑ Bouma, R. J.; Teuben, J. H.; Beukema, W. R.; Bansemer, R. L.; Huffman, J. C.; Caulton, K. G. (1984). »Identification of the Zinc Reduction Product of VCl3 · 3THF as [V2Cl3(THF)6]2[Zn2Cl6]«. Inorganic Chemistry. 23 (17): 2715–2718. doi:10.1021/ic00185a033.
- ↑ Irish, D. E.; McCarroll, B.; Young, T. F. (1963). »Raman Study of Zinc Chloride Solutions«. The Journal of Chemical Physics. 39 (12): 3436–3444. doi:10.1063/1.1734212.
- ↑ Yamaguchi, T.; Hayashi, S.; Ohtaki, H. (1989). »X-Ray Diffraction and Raman Studies of Zinc(II) Chloride Hydrate Melts, ZnCl2 · RH2O (R = 1.8, 2.5, 3.0, 4.0, and 6.2)«. The Journal of Physical Chemistry. 93 (6): 2620–2625. doi:10.1021/j100343a074.
- ↑ Pye, C. C.; Corbeil, C. R.; Rudolph, W. W. (2006). »An ab initio Investigation of Zinc Chloro Complexes«. Physical Chemistry Chemical Physics. 8 (46): 5428–5436. doi:10.1039/b610084h. ISSN 1463-9076. PMID 17119651.
{{navedi časopis}}: Vzdrževanje CS1: več imen: seznam avtorjev (povezava) - ↑ Brown, I. D. (2006). The Chemical Bond in Inorganic Chemistry: The Bond Valence Model. Oxford University Press. ISBN 0-19-929881-5.
- ↑ Zhang, X. G. (1996). Corrosion and Electrochemistry of Zinc. Springer. ISBN 0-306-45334-7.
- ↑ Vulte, H. T. (2007). Laboratory Manual of Inorganic Preparations. Read Books. ISBN 1-4086-0840-5.
- ↑ Shriner, R. L.; Ashley, W. C.; Welch, E. (1955). »2-Phenylindole« (PDF). Org. Synth.
{{navedi revijo}}: Vzdrževanje CS1: več imen: seznam avtorjev (povezava); Coll. Vol., zv. 3, str. 725 - ↑ Cooper, S. R. (1955). »Resacetophenone« (PDF). Org. Synth.; Coll. Vol., zv. 3, str. 761
- ↑ Dike, S. Y.; Merchant, J. R.; Sapre, N. Y. (1991). »A New and Efficient General Method for the Synthesis of 2-Spirobenzopyrans: First Synthesis of Cyclic Analogues of Precocene I and Related Compounds«. Tetrahedron. 47 (26): 4775–4786. doi:10.1016/S0040-4020(01)86481-4.
{{navedi časopis}}: Vzdrževanje CS1: več imen: seznam avtorjev (povezava) - ↑ Furnell, B. S. (1989). Vogel's Textbook of Practical Organic Chemistry (5th izd.). New York: Longman/Wiley.
- ↑ Bauml, E.; Tschemschlok, K.; Pock, R.; Mayr, H. (1988). »Synthesis of γ-Lactones from Alkenes Employing p-Methoxybenzyl Chloride as +CH2-CO2- Equivalent« (PDF). Tetrahedron Letters. 29 (52): 6925–6926. doi:10.1016/S0040-4039(00)88476-2.
{{navedi časopis}}: Vzdrževanje CS1: več imen: seznam avtorjev (povezava) - ↑ Predloga:Navaja revija
- ↑ House, H. O.; Crumrine, D. S.; Teranishi, A. Y.; Olmstead, H. D. (1973). »Chemistry of Carbanions. XXIII. Use of Metal Complexes to Control the Aldol Condensation«. Journal of the American Chemical Society. 95 (10): 3310–3324. doi:10.1021/ja00791a039.
{{navedi časopis}}: Vzdrževanje CS1: več imen: seznam avtorjev (povezava)