Amonijev ion

| |
| Imena | |
|---|---|
| Druga imena
amonijev kation, protonirani amonijak
| |
| Identifikatorji | |
3D model (JSmol)
|
|
CompTox Dashboard (EPA)
|
|
| |
| Lastnosti | |
| NH4+ | |
| Videz | brezbarven |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Amonijev ion (tudi amonijev kation) je pozitivno nabiti poliatomski kation s kemijsko formulo NH4+. Molska masa znaša 18,05 g/mol, pKa pa znaša 9,25. Amonijev ion nastane s protonacijo amonijaka (NH3).
Amonijeve spojine imajo številne komercialne uporabe, kot je npr. amonijev nitrat(V) oz. amonijev soliter (NH4NO3), ki se uporablja kot surovina za gnojila in eksplozive.
Amonijev ion je za organizme toksičen, zato so le-ti razvili različne načine izločanja: ribe in drugi vodi organizmi ga izločajo neposredno v vodo, sesalci in dvoživke v obliki sečnine, ptiči in plazilci pa v obliki sečne kisline.
Kemijske lastnosti in reakcije[uredi | uredi kodo]
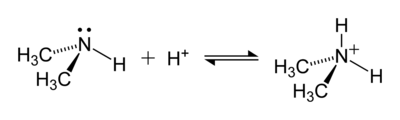
Amonijev nastane pri reakciji med amonijakom, ki predstavlja šibko bazo in neko kislino, ki predstavlja donorja protonov:
pri čemer predstavlja dvopičje (:) na dušikovem atomu (N) nevezni elektronski par, ki z vodikovim protonom tvori koordinativno kovalentno vez.
Amonijev ion je močna konjugirana kislina in lahko reagira z neko bazo, pri čemer pride torej do deprotonacije in posledično nastanka amonijaka:
Pri raztapljanju amonijak v vodi znaten delež reagira z oksonijevim ionom, pri čemer tudi nastanejo amonijevi ioni:
Količina nastalega iona je odvisna od pH vrednosti raztopine. V primeru nizkega pH, tj. pri visoki koncentraciji oksonijevih ionov, je ravnotežje reakcije pomaknjeno v desno, s tem pa je torej več molekul amonijaka protoniranih. Če je pH visok, pride do obratne situacije, tj. ravnotežje je pomaknjeno v levo in tako nastane več molekul amonijaka.

Reakcije lahko potekajo tudi v plinasti fazi: primer tega je reakcija med vodikovim kloridom in NH4+ v plinastih stanjih, pri čemer nastane beli oblak amonijevega klorida (NH4Cl), ki nato preide v trdno stanje. NH4+ so podobni ionom alkalijskih kovin, kot sta natrijev (Na+) in kalijev kation (K+). Večina enostavnih amonijevih soli je dobro topna v vodi.[1]
Pri redukciji NH4+ nastaneta amonijak in vodik:
Pri elektrolizi amonijevega klorida z živosrebrovo elektrodo pri temperaturi 0°C nastane siva masa, podobna natrijevemu ali kalijevemu amalgamu. Pri segrevanju začne razpadati na amonijak in vodik.[1] This amalgam spontaneously decomposes to give ammonia and hydrogen.[2]
Substituirani amonijevi ioni[uredi | uredi kodo]
Vsak vodikvo atom v amonijevem ionu je lahko nadomeščen z alkilno skupino ali kakšno drugo organsko skupino, pri čemer nastane substituiran amonijev ion, imenovan tudi aminijev ion. Glede na število organskih skupin poznamo primarne, sekundarne, terciarne in kvartarne amonijeve ione.
Tovrstni ion lahko nastane npr. pri reakciji med dimetilaminom in neko kislino, pri čemer nastane dimetilaminijev kation (CH3)2NH2+:
Pri kvartarnih amonijevih ionih so na dušikov atom vezane štiri organske skupine. Vodikov atom, ki bi ga lahko prevzela baza, je odsoten, zato so ioni trajno nabiti. Takšni kationi, kot je tetra-n-butilamonijev kation, so včasih uporabljeni za zvečanje topnosti neke snovi v organskih topilih namesto kalijevih in natrijevih kationov.
Amonijeve spojine[uredi | uredi kodo]
Ravnotežje raztopine amonijaka v vodi (salmiakovec, salmiakov cvet) lahko zapišemo tudi kot:
Raztopina vsebuje torej ione amonijevega hidroksida in je šibka baza. Uporablja se za nevtralizacijo kislin, kot sredstvo za raztapljanje bakrovega oksida (CuO) v tekočih čistilih za kovine ter kot gnojilo.
Amonijev klorid (NH4Cl, salmiak) se uporablja pri spajkanju, za suhe galvanske člene, kot gnojilo ter kot zdravilo proti bronhialnemu katarju (vnetje bronhov, ki povzroča pretežno močen vdor serozne tekočine).[3]
Amonijev sulfat(VI), (NH4)2SO4, pridobivajo z uvajanjem ogljikovega dioksida (CO2) v amoniakalno suspenzijo mavca ali anhidrita. Je splošno znano gnojilo (žveplenokisli amonijak), uporablja pa se tudi kot vir dušika pri proizvodnji kvasa ter kot sredstvo za zaščito papirja pred ognjem.[3]
Amonijev nitrat(V) (NH4NO3, amonijev soliter) nastane iz amonijaka in dušikove(V) kisline, uporablja pa se kot surovina za gnojila in eksplozive. Pri segrevanju oddaja smejalni plin (N2O).[3]
Amonijev hidrogenkarbonat (NH4HCO3) poleg amonijevega karbamata (NH2-CO-ONH4) je sestavina t. i. jelenove soli, ki se uporablja kot pecilni prašek.[3]
Amonijev ion v organizmih[uredi | uredi kodo]

Amonijev ion je toksičen odpadni produkt presnove v živalih. Ribe in vodni nevretenčarji izločajo ion neposredno vodo zaradi njegove dobre topnosti. Sesalci, morski psi in dvoživke ga pretvorijo preko cikla sečnine v sečnino (ureo), saj je le-ta manj toksična za organizem in se lažje shranjuje. Ptiči, plazilci in kopenske kače pretvorijo ion v sečno kislino, ki je v trdnem stanju, in se jo lahko izloči z minimalno izgubo vode; to omogoča živalim učinkovito zadržanje vode v suhem in vročem okolju.[4]
Toksičnost[uredi | uredi kodo]
Molekulska osnova toksičnosti amonijaka oz. amonijevega iona ni popolnoma znana. Kljub temu je znano, da so glavni prizadeti organ možgani. Namreč, glavno vlogo pri odstanjevanju amonijevih ionov imata aminokislini glutamat in glutamin. Encim glutamat dehidrogenaza katalizira reduktivno aminacijo α-ketoglutarata, pri čemer nastane glutamat, glutamin sintetaza pa nato katalizira pretvorbo glutamata v glutamin. Pri zelo visokih koncentracijah NH4+ se zviša tudi raven glutamina, ki v astrocitih deluje kot osmotsko aktiven delec. Zaradi tega pride do velikega privzema vode v te celice, pri tem pa naraste intrakranialni (znotrajlobanjski) pritisk, kar vodi v komatozno stanje (stanje globoke nezavesti, iz katere bolnika ni mogoče prebuditi). V skladu z visoko koncentracijo ionov se pri reduktivni aminaciji porabijo tudi velike količine α-ketoglutarata, ki je hkrati pomemben intermediat v Krebsovem ciklu. Njegovo pomanjkanje vodi torej v pomanjkanje visokoenergetskih prenašalcev elektronov (NADH in FADH2), v končni fazi pa se zmanjša proizvodnja adenozin trifosfata (ATP) pri oksidativni fosforilaciji. Poleg tega sta glutamat in njegov derivat, γ-aminomaslena kislina (GABA) pomembna živčna prenašalca (nevrotransmiterja), zmanjšanje njune ravni pa lahko dodatno vodi v različna nevropsihološka stanja.[5][6]
Sama reakcija raztapljanja amonijaka v vodi, pri čemer nastane amonijev hidroksid, je eksotermna in je najpogostejši način, preko katerega pride do poškodbe (tj. kemične opekline) kože, oči in še posebej sluznice dihal.[7]
Amonijevi ioni so v prevelikih količinah toksični tudi za rastline, navkljub dejstvu, da so ioni lahko pomembni vir dušika.[8]
Glej tudi[uredi | uredi kodo]
Opombe in reference[uredi | uredi kodo]
- ↑ 1,0 1,1 Pseudo-binary compounds Arhivirano 2020-07-27 na Wayback Machine. Pridobljeno 15. 03. 2010.
- ↑ »Ammonium Salts«. VIAS Encyclopedia. 15. marec 2010.
- ↑ 3,0 3,1 3,2 3,3 Schröter W., Lautenschläger K.-H., Bibrack H. in Schnabel A. ([1990] 1993). KEMIJA, Splošni priročnik. Ljubljana: Tehniška založba Slovenije, str. 376-7. ISBN 86-365-0122-9
- ↑ Campbell, N.A.; Reece, J.B. (2002). »44«. Biology (6. izd.). San Francisco, Kalifornija: Pearson Education, Inc. str. 937–938. ISBN 0-8053-6624-5.
- ↑ Nelson, D.L. & Cox, M.M. (2008). Lehninger Principles of Biochemistry, 5. izdaja. NY: W.H. Freeman and Company, str. 681-2. ISBN 978-1-4292-0892-5
- ↑ Devlin, T.M. (2002). Textbook of biochemistry with clinical correlations, 5. izdaja. New York: Wiley-Liss. ISBN 0-471-41136-1
- ↑ Issley, S. (2009). Ammonia Toxicity. emedicine. Pridobljeno 15. 03. 2010.
- ↑ Britto, D.T. & Kronzucker, H.J. (2002). »NH4+ toxicity in higher plants: A critical review«. J. Plant. Physiol. 159: 567-584.