Koordinacijsko število
V kemiji in kristalografiji je koordinacijsko število centralnega atoma v molekuli ali kristalu število njegovih najbližjih sosedov. Koordinacijsko število se za molekule določa nekoliko drugače kot za kristale.
V kemiji je poudarek na strukturah vezi v molekulah ali ionih, zato se koordinacijsko število določa preprosto s seštevanjem atomov, ki so z enojnimi ali večkratnimi vezmi vezani na centralni atom. Primer: v kompleksnem ionu [Cr(NH3)2Cl2Br2]1- ima centralni kation Cr3+ koordinacijsko število 6, ker je nanj vezanih šest skupin: dve skupini NH3 in po dva iona Cl- in Br-.
V strukturah trdnega stanja, na primer v kristalih, so kemijske vezi pogosto definirane manj jasno, zato se zanje uporabljajo enostavnjejši modeli, v katerih so atomi prikazani kot toge, stikajoče se kroglice. V teh modelih je koordinacijsko število atoma število atomov, s katerimi se stika.
Uporaba v kemiji[uredi | uredi kodo]
V kemiji je koordinacijsko število prvi definiral Alfred Werner leta 1893 kot celotno število sosedov centralnega atoma v molekuli ali ionu.[1][2] Primer: ogljikov atom ima v večini stabilnih organskih spojin po štiri vezi, njegovo koordinacijsko število pa je lahko različno. V metanu (CH4) je enako štiri, ker so nanj vezani štirje vodikovi atomi, v etenu (CH2=CH2) tri, ker so nanj vezani en ogljikov in dva vodikova atoma, v etinu (CH≡CH) pa dva, ker sta nanj vezana en ogljikov in en vodikov atom. Za računanje koordinacijskega števila se šteje samo prva (sigma) vez, druga in tretja (pi) vez pa ne.
Tudi v anorganski kemiji se šteje samo prva ali sigma vez med vsakim ligandom in centralnim atomom, ne pa tudi pi vezi istih ligandov. V volframovem heksakarbonilu (W(CO)6) je koordinacijsko število volframa enako šest, čeprav so v kovinskih karbonilih pomembne tako sigma kot pi vezi.
Kompleksi z visokimi koordinacijskimi števili so na primer ioni, ki jih tvorita uran in torij z dvodentatnimi nitratnimi ioni kot ligandi. Takšna iona sta na primer U(NO3)62− in Th(NO3)62−, v katerih je vsak nitratni ligand vezan na kovino preko dveh kisikovikovih atomov, tako da je koordinacijsko število urana oziroma torija enako 12.
Če so ionski polmeri ligandov majhni, so možna tudi večja koordinacijska števila. Ena od računalniških študij je napovedala posebno stabilen ion PbHe152+, ki je zgrajen iz centralnega svinčevega iona, koordiniranega z nič manj kot 15 helijevimi atomi.[3]
Uporaba v kristalografiji[uredi | uredi kodo]

V materialnih znanostih je koordinacijsko število danega atoma v notranjosti kristalne rešetke enako številu atomov, ki se ga dotikajo. Železo pri 20 °C kristalizira kot telesno centrirana kocka, v kateri je vsak notranji železov atom obdan z osmimi sosednjimi železovimi atomi. Koordinacijsko število strukture je zato enako 8.
Najvišje koordinacijsko število je 12. Pojavlja se v heksagonalnem gostem zlogu in kubičnem gostem zlogu oziroma v ploskovno centrirani kocki. Koordinacijsko število 12 ustreza teoretični zgornji meji kontaktnega števila za enako velike kroglice.

Najbolj znana alotropa ogljika imata različni koordinacijski števili. V diamantu je vsak ogljikov atom v središču tetraedra, ki ga tvorijo drugi štirje ogljikovi atomi. Koordinacijsko število je zato enako 4, tako kot v metanu. Grafit je zgrajen iz dvodimenzionalnih slojev, v katerih je vsak ogljikov atom vezan na tri sosednje ogljikove atome. Atomi na drugih slojih so bolj oddaljeni in niso najbližji sosedje. Koordinacijsko število ogljika je zato enako 3, kot v etenu.
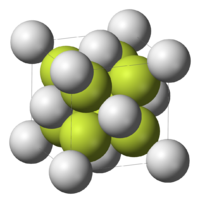
Enostavne ionske strukture so opisane z dvema koordinacijskima številoma za vsak ion posebej. Kalcijev fluorid ima strukturo (8,4). To pomeni, da je vsak kation Ca2+ obkrožen z osmimi anioni F- in vsak anion F- s štirimi kationi Ca2+. V natrijevem kloridu (NaCl) je število kationov in anionov enako, zato sta enaki tudi obe koordinacijski števili (6,6).
Koordinacijsko število atoma, ki je na površini kristala, je vedno manjše od kordinacijskega števila atoma v notranjosti krisala in je odvisno od Millerjevih indeksov ploskve. V telesno centriranem kubičnem kristalu je koordinacijsko število atoma na ploskvi (100) enako 4.
Sklici[uredi | uredi kodo]
- ↑ De, A.K: "A Text Book of Inorganic Chemistry", str. 88. New Age International Publishers, 2003.
- ↑ IUPAC, Compendium of Chemical Terminology, 2. izd. (the "Gold Book") (1997). Spletna izdaja: (2006–) "coordination number". DOI: 10.1351/goldbook.C01331
- ↑ The Search for the Species with the Highest Coordination Number Andreas Hermann, Matthias Lein, and Peter Schwerdtfeger, Angew. Chem. Int. Ed. (2007), 46, str. 2444–2447
Vir[uredi | uredi kodo]
- R. Hoppe: Die Koordinationszahl - ein „anorganisches Chamäleon“. Angewandte Chemie 82(1), (1970), str. 7-16 ISSN 0044-8249
