Vodikov klorid
| |||
| Imena | |||
|---|---|---|---|
| IUPAC ime
Vodikov klorid[1]
| |||
| Druga imena
Klorovodik
Hidroklorid | |||
| Identifikatorji | |||
3D model (JSmol)
|
|||
| 1098214 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.723 | ||
| EC število |
| ||
| Gmelin | 322 | ||
| KEGG | |||
PubChem CID
|
|||
| RTECS število |
| ||
| UNII | |||
| UN število | 1050 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Lastnosti | |||
| ClH | |||
| Molska masa | 36,46 g·mol−1 | ||
| Videz | Brezbarven plin | ||
| Vonj | Jedek | ||
| Gostota | 1,490 g L−1[2] | ||
| Tališče | −11.422 °C (−20.528 °F; −11.149 K) | ||
| Vrelišče | −8.505 °C (−15.277 °F; −8.232 K) | ||
| Parni tlak | 4352 kPa (pri 21,1 °C)[3] | ||
| Kislost (pKa) | -7,0[4] | ||
| Bazičnost (pKb) | 21,0 | ||
| Lomni količnik (nD) | 1,0004456 (plin) | ||
| Struktura | |||
| Oblika molekule | Linearna | ||
| Dipolni moment | 1,05 D | ||
| Termokemija | |||
| Specifična toplota, C | 0,7981 J K−1 g−1 | ||
| Standardna molarna entropija S |
186,902 J K−1 mol−1 | ||
Std tvorbena
entalpija (ΔfH⦵298) |
–92,31 kJ mol−1 | ||
Std sežigna
entalpija (ΔcH⦵298) |
–95,31 kJ mol−1 | ||
| Nevarnosti | |||
| GHS piktogrami |  
| ||
| Opozorilna beseda | Pozor | ||
| H280, H314, H331 | |||
| P261, P280, P305+351+338, P310, P410+403 | |||
| NFPA 704 (diamant ognja) | |||
| Smrtni odmerek ali koncentracija (LD, LC): | |||
LD50 (srednji odmerek)
|
238 mg/kg (podgane, zaužitje) | ||
| Sorodne snovi | |||
| Sorodne snovi | Vodikov fluorid | ||
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |||
| Sklici infopolja | |||
Vodikov klorid je kemijska spojina vodika in klora s formulo HCl. Pri sobni temperaturi je brezbarven jedek plin, ki z vlago iz zraka tvori belo paro klorovodikove kisline. Vodikov klorid in klorovodikova kislina sta pomembni industrijski surovini. Kemijska formula HCl se pogosto napačno uporablja, kot formula klorovodikove kisline, vendar ja zato potrebno natančnejše označevanje. Klorovodikova kislina je raztopina vodikovega klorida v vodi, zato jo označujemo kot HCl (aq). Plin vodikov klorid pa samo HCl, lahko pa tudi kot HCl (g).
Kemija[uredi | uredi kodo]

Vodikov klorid ima dvoatomne molekule, v katerih sta vodik in klor vezana z enojno kovalentno vezjo. Ker je klor mnogo bolj elektronegativen od vodika, je vez zelo polarna in ima zato velik dipolni moment z negativnim delnim nabojem δ– na klorovem atomu in pozitivnim delnim nabojem δ+ na vodikovem atomu. HCl je (tudi) zaradi velike polarnosti dobro topen v vodi in drugih polarnih topilih.
V vodnih raztopinah tvori hidronijeve katione in kloridne anione. Reakcija je reverzibilna:
- HCl + H2O → H3O+ + Cl–
Nastala raztopina je močna klorovodikova kislina. Njena disociacijska oziroma ionizacijska konstanta Ka je velika (pKa=-8,0), kar pomeni, da v vodi popolnoma disociira ozirom ionizira. Vodikov klorid tudi v odsotnosti vode deluje kot kislina: lahko se raztaplja v nekaterih polarnih topilih, na primer v metanolu, protonira molekule ali ione in deluje kot kisli katalizator v kemijskih reakcijah, v katerih se zahtevajo brezvodni pogoji.
- HCl + CH3OH → CH3O+H2 + Cl–
Vodikov klorid je zaradi svojih kislih lastnosti zelo koroziven, predvsem v prisotnosti vlage.
Zgradba in lastnosti molekule[uredi | uredi kodo]
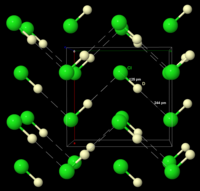
Na zgornjih slikah je prikazana zgradba DCl, določena z nevtronsko difrakcijo uprašenega DCl pri temperaturi 77K. DCl se je uporabil namesto HCl zato, ker je jedra devterija laže odkriti kot jedra vodika. S prekinjeno črto so nakazane neskončne verige DCl.
| Temperatura (°C) | 0 | 20 | 30 | 50 |
|---|---|---|---|---|
| Voda | 823 | 720 | 673 | 596 |
| Metanol | 513 | 470 | 430 | |
| Etanol | 454 | 410 | 381 | |
| Eter | 356 | 249 | 195 |
Rentgenska difrakcija uprašenega trdnega HCl je pokazala, da pri temperaturi 98,4 K preide iz ortorombske v kubično kristalno strukturo. Klorovi atomi so v obeh strukturah na ploskovno centriranem področju. Položaja vodikovih atomov se ne da določiti.[6] Analiza spektroskopskih in dielektričnih podatkov in določitev strukture DCl kažejo, da HCl v trdnem stanju tvori žagasto verigo, podobno kot HF.[7]


Infrardeči spekter plinastega HCl je sestavljen iz številnih ostrih absorbcijskih črt, grupiranih okoli 2886 cm−1 (valovna dolžina ~3,47 µm). Pri sobni temeraturi so skoraj vse molekule v osnovnem vibracijskem stanju v = 0. Pri prehodu molekule v stanje v = 1 bi pričakovali vidno absorbcijsko črto pri približno 2880 cm-1. Ta absorbcijska črta, ki ustreza veji Q, ni opažena, ker je nedopustna zaradi simetrije. Namesto nje se zaradi rotacije molekul pojavljata dva niza signalov (veji P in R). Zaradi pravil kvantne mehanike so dopustni samo nekateri načini rotacije. Zanje so značilna rotacijska kvantna števila J = 0, 1, 2, 3 ... ΔJ ima lahko vrednosti samo ± 1.
- E(J) = h•B•J(J+1)
Ker je vrednost B veliko manjša od v e, je za rotacijo molekule potrebna zelo majhna količina energije, ki za značilno molekulo leži v mikrovalovnem področju. Vibracijska energija molekule HCl ima absorbcijo na infrardečem področju, zato se vibracijski spekter molekule zlahka zbere z običajnim infrardečim spektrometrom s konvencionalno plinsko celico.
Naravni klor vsebuje izotopa 35Cl in 37Cl v razmerju približno 3:1. Njuni konstanti vzmeti sta zelo podobni, reducirani masi pa sta različni, kar povzroči znatne razlike v rotacijski energiji. Pri podrobnem pregledu vsake absorbcijske črte se zato opazi dublet v enakem razmerju 3:1.
Pridobivanje[uredi | uredi kodo]
Večina industrijsko proizvedenega vodikovega klorida se uporabi za proizvodnjo klorovodikove kisline.
Laboratorijske metode[uredi | uredi kodo]
Majhne količine plinastega HCl za laboratorijske potrebe se lahko proizvede v generatorju HCl z dehidriranjem klorovodikove kisline z žveplovo kislino (H2SO4) ali brezvodnim kalcijevim kloridom (CaCl2). Druga možnost je reakcija med žveplovo kislino in natrijevim kloridom (NaCl):[8]
- NaCl + H2SO4 → NaHSO4 + HCl
Reakcija poteka že pri sobni temperaturi. Pri temperaturah nad 200 C poteka med suhimi ostanki NaCl in nastalim NaHSO4 naslednja reakcija:
- NaCl + NaHSO4 → HCl + Na2SO4
HCl se lahko pripravi tudi s hidrolizo nekaterih reaktivnih kloridov, na primer fosforjevih kloridov, tionil klorida (SOCl2) in acil kloridov. HCl se na primer iz fosforjevega pentaklorida (PCl5) proizvede tako, da na klorid počasi kaplja hladna voda, pri čemer poteka naslednja reakcija:
- PCl5 + H2O → POCl3 + 2 HCl
Plin se mora v tem primeru hraniti v majhnih tlačnih posodah ali valjih, ki so lahko dragi. Za druge postopke pridobivanja zadostuje običajna laboratorijska oprema.
Neposredna sinteza[uredi | uredi kodo]
Med elektrolizo vodne raztopine natrijevega klorida nastajajo klor (Cl2), natrijev hidroksid (NaOH) in vodik (H2). Nastali vodik lahko s klorom zgori v vodikov klorid:
- Cl2(g) + H2(g) → 2 HCl(g)
Reakcija je eksotermna. Nastali plinasti vodikov klorid se absorbira v deionizirani vodi, tako da nastane klorovodikova kislina. Reakcija daje zelo čist proizvod, uporaben tudi v prehrambeni industriji.
V Sloveniji HCl z neposredno sintezo proizvaja TKI Hrastnik.[9]
Organske sinteze[uredi | uredi kodo]
Največja industrijska proizvodnja vodikovega klorida je povezana s proizvodnjo kloriranih in fluoriranih organskih spojin, na primer teflona, freona in drugih kloriranih ogljikovodikov ter klorocetne kisline in PVC. V proces je pogosto vključena tudi proizvodnja klorovodikove kisline.
Med sintezo omenjenih spojin se vodikov atom v ogljikovodikih zamenja z atomom klora. Odcepljeni atom vodika se spaja z drugim atomom iz molekule klora, tako da nastane vodikov klorid. Vodikov klorid nastaja tudi med kasnejšim fuoriranjem kloriranih ogljikovodikov:
- R-H + Cl2 → R-Cl + HCl
- R-Cl + HF → R-F + HCl
Nastali vodikov klorid se lahko ponovno uporabi ali absorbira v vodi, pri čemer nastane klorovodikova kislina tehnične oziroma industrijske kakovosti.
Uporaba[uredi | uredi kodo]
Večina vodikovega klorida se uporabi s proizvodnjio klorovodikove kisline. Uporablja se tudi za industrijsko hidrokloriranje gume in proizvodnjo vinilnih in alkilnih kloridov.
V industriji polprevodnikov se uporablja za jedkanje kristalov polprevodnikov in rafiniranje silicija preko triklorosilana (SiHCl3).
Uporablja se tudi za odstranjevanje bombažnih vlaken in ločevanje bombaža od volne.
V laboratoriju je absolutno suh vodikov klorid še posebno uporaben za pripravo Lewisovih kislin.
Zgodovina[uredi | uredi kodo]
Alkimisti so že v srednjem veku ugotovili, da klorovodikova kislina, imenovana spiritus salis ali acidum salis, sprošča vodikov klorid, ki so ga imenovali kisli morski zrak. V 17. stoletju je Johann Rudolf Glauber iz kuhinjske soli in žveplove kisline pripravil natrijev sulfat (Na2SO4), pri čemer se je sproščal plinasti HCl. Leta 1772 sta o isti reakciji poročala tudi Carl Wilhelm Scheele in Joseph Priestley in leta 1810 je Humphry Davy ugotovil, da je sestavljen iz vodika in klora.[10]
Med industrijsko revolucijo je začela naraščati potreba po alkalnih kemikalijah, na primer sodi (Na2CO3), zato je Nicolas Leblanc razvil industrijski postopek za njeno proizvodnjo. V Leblancovem postopku se kuhinjska sol s pomočjo žveplove kisline, apnenca in oglja pretvori v vodikov klorid. Plin se je prvotno izpučal v zrak, dokler ni bil leta 1863 v Angliji sprejet Akt o alkalijah, ki je izpuste prepovedal. Proizvajalci sode so zatem odpadni plin raztapljali v vodi in v industrijskem obsegu proizvajali klorovodikovo kislino. Kasneje se je soda proizvajala tudi po Hargreavesovem postopku, ki je podoben Leblancovemu, samo da so se namesto žveplove kisline uporabljali žveplov dioksid (SO2), voda in zrak. V zgodnjem 20. stoletju se je uveljavil Solvayev postopek za proizvodnjo sode, v katerem ni stranskega proizvoda HCl.
Vodikov klorid se je v 20. stoletju uporabljal za hidrokloriranje alkinov. Na ta način sta se proizvajala monomera kloropren in vinil klorid, ki sta se zatem polimerizirala v polikloropren (sintetični gumij neopren) in polivinil klorid (PVC). V proizvodnji vinil klorida se je acetilen (etin, C2H2) hidrokloriral s HCl, pri čemer je ena vez v trojni vezi razpadla in prešla v dvojno vez:
- HC≡CH + HCl → H2C=CHCl
Acetilenski postopek za proizvodnjo kloroprena se je uporabljal do 1960. let. Prvi korak v procesu je bila dimerizacija etina, drugi korak pa adicija klorovodika na preostalo trojno vez:
Acetilenski postopek je nadomestil postopek, v katerem se najprej na eno od dvojnih vezi v 1,3-butadienu adira klor in zatem eliminira HCl:
- H2C=CH-CH=CH2 + Cl2 → H2C=CH-CHCl-CH2Cl
- H2C=CH-CHCl-CH2Cl → H2C=CH-CCl=CH2 + HCl
Varnost[uredi | uredi kodo]
Vodikov klorid v stiku z vodo v tkivu tvori zelo jedko klorovodikovo kislino. Vdihavanje par lahko povzroči kašljanje, dušenje in vnetje nosu, grla in gornjih dihalnih poti. Pri težjih zastrupitvah povzroči pljučni edem, razpad obtočil in smrt. Pri stiku s kožo povzroči rdečico, bolečino in težke opekline. Pri stiku z očmi lahko povzroči trajne okvare vida.
Plin je zelo hidrofilen in se iz izpušnih plinov zlahka izpere s prepihavanjem skozi vodo. Stranski proizvod je klorovodikova kislina.
Oprema za ravnanje z vodikovim kloridom mora biti preverjena, še posebno ventili in regulatorji. Izdelana mora biti iz izbranih gradiv, na primer iz nerjavnega jekla ali polimerov.
Sklici[uredi | uredi kodo]
- ↑ »Hydrogen chloride (CHEBI:17883)«. Chemical Entities of Biological Interest (ChEBI). UK: European Bioinformatics Institute.
- ↑ W.M.Haynes (2010), Handbook of Chemistry and Physics (91. izdaja), Boca Raton, Florida: CRC Press. str. 4–67. ISBN 978-1-4398-2077-3.
- ↑ Hydrogen Chloride Arhivirano 2014-02-22 na Wayback Machine.. Gas Encyclopaedia. Air Liquide
- ↑ D. D. Perrin, Dissociation constants of inorganic acids and bases in aqueous solution, Butterworths, London, 1969.
- ↑ Hydrochloric Acid - Compound Summary. Pubchem
- ↑ G. Natta (1933), Struttura e polimorfismo degli acidi alogenidrici, Gazzetta Chimica Italiana, 63, str. 425–439.
- ↑ E. Sándor, R. F. C. Farrow (1967), Crystal Structure of Solid Hydrogen Chloride and Deuterium Chloride, Nature, 213, str. 171–172, DOI 10.1038/213171a0.
- ↑ Francisco J. Arnsliz (1995). »A Convenient Way To Generate Hydrogen Chloride in the Freshman Lab«. J. Chem. Ed. 72 (12): 1139. doi:10.1021/ed072p1139. Arhivirano iz prvotnega spletišča dne 24. septembra 2009. Pridobljeno 23. maja 2012.
- ↑ TKI Hrastnik d.d.
- ↑ Hartley, Harold (1960). »The Wilkins Lecture. Sir Humphry Davy, Bt., P.R.S. 1778–1829«. Proceedings of the Royal Society of London (A). 255 (1281): 153–180. Bibcode:1960RSPSA.255..153H. doi:10.1098/rspa.1960.0060.