Trehaloza

| |
| |

| |
| Imena | |
|---|---|
| IUPAC ime
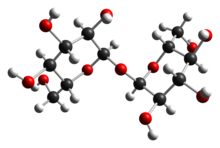
2-(hidroksimetil)-6-[3,4,5-trihidroksi-6-(hidroksimetil)
tetrahidropiran-2-yl]oxy-tetrahidropiran-3,4,5-triol C12H22O11•2H2O (dihidrat) | |
| Druga imena
α-D-glukopiranosil α-D-glukopiranosid(α,α‐Trehaloza)
| |
| Identifikatorji | |
| ECHA InfoCard | 100.002.490 |
PubChem CID
|
|
CompTox Dashboard (EPA)
|
|
| Lastnosti | |
| C12H22O11 (brezvodni) | |
| Molska masa | 342.296 g/mol (brezvodni) 378.33 g/mol (dihidrat) |
| Videz | Beli ortorombski kristali |
| Gostota | 1.58 g/cm3 pri 24 °C |
| Tališče | 203 °C (brezvodni) 97 °C (dihidrat) |
| 68.9 g na 100 g raztopine pri 20 °C[1] | |
| Topnost | topen v etanolu , netopen v dietil etru in benzenu[2] |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Trehaloza poznana tudi kot mikoza ali tremaloza, je naravni alfa disaharid, kjer sta dve α- glukozni enoti povezani z α, α-1, 1- glikozidno vezjo. Leta 1832 je Wiggers odkril trehalozo v rženih rožičkih, leta 1859 pa je Berthelot izoliral trehalozo iz »trehala manna«, snovi ki jo proizvajajo hrošči rilčkarji in jo poimenoval trehaloza. Trehalozo lahko sintetizirajo glive, rastline in nevretenčarji. Trehaloza je vključena v anhidrobiozo, to je sposobnost rastlin in živali, da prenesejo daljša obdobja izsušitve. Ima visoko zmogljivosti zadrževanja vode in se uporablja v živilih in kozmetičnih izdelkih.
Ko celica izgublja vodo (dehidrira), naj bi trehaloza tvorila gelsko fazo in s tem preprečila poškodbo celičnih organelov. Rehidracija nato omogoča, da se normalna celična dejavnost nadaljuje brez večje oziroma letalne škode, ki navadno sledi v dehidracijsko rehidracijskemu ciklu. Trehaloza je antioksidant, kar predstavlja dodatno prednost. Ekstrakcija trehaloze je bila težaven in drag proces, dokler ni družba Hayashibara (Okayama, Japonska) zasnovala poceni tehnologije ekstrakcije iz škroba, za množično proizvodnjo. Trehaloza se trenutno uporablja za širok spekter aplikacij.
Struktura[uredi | uredi kodo]
Trehaloza je disaharid, ki nastane s tvorbo 1,1-glikozidne vezi med dvema α-glukoznima enotama. Glikozidna vez nastane iz dveh reduciranih oblik glukoze, zato ne more reducirati drugih spojin.
Kemijske lastnosti[uredi | uredi kodo]
Trehaloza je bila prvič izolirana iz rženih rožičkov. Emil Fisher je prvi opisal tehaloza-hidrolizni encim v kvasu. Trehaloza je nereducirajoči sladkor iz dveh glukoznih enot, med katerima se tvori 1,1-α vez, zato se imenuje α-D-glukopiranozil-(1 → 1)-α-D-glukopiranozid. Tako nastala vez daje trehalozi veliko odpornost proti kisli hidrolizi zato je stabilna v raztopini tako pri visoki temperaturi, kot tudi v kislih pogojih. Glikozidna vez ohrani nereducirajoči sladkor v zaprti obliki obroča, tako da se ne more vezati preko aldehidne ali ketonske skupine na lizinske ali argininske ostanke proteinov (proces glikacije oziroma ne encimske glikozilacije). Encim trehalaza cepi sladkor trehalozo v dve molekuli glukoze. Trehaloza ima približno 45% sladkosti saharoze in je manj topna od saharoze, razen pri visokih temperaturah (> 80 °C). Trehaloza je v kristalu dihidrat z romboidno obliko in ima 90% kalorične vsebnosti saharoze v tej obliki. Brezvodna oblika trehaloze zlahka veže vlago in preide v obliko dihidrata. Brezvodna oblika trehaloze lahko pokaže zanimive fizikalne lastnosti, kadar je toplotno obdelana.
Biološke lastnosti[uredi | uredi kodo]
V naravi najdemo trehalozo v živalih, rastlinah in mikroorganizmih. V živalih se največ trehaloze nahaja v kozicah in žuželkah, pri katerih je trehaloza krvni sladkor (kobilice, metulji in čebele). V rastlinah je največ trehaloze prisotne v sončničnih semenih in morskih algah, kjer služi kot vir energije in ogljika. V kvasovkah in rastlinah ima lahko vlogo signalne molekule, ki nadzira določene metabolične procese in celo rast. Trehaloza lahko zaščiti proteine in celične membrane pred inaktivacijo ali denaturacijo povzročeno z raznimi stresnimi pogoji npr. dehidracijo, izsušitvijo, vročino, mrazom in oksidacijo. V družini gliv je prisotna v nekaterih gobah, ki lahko vsebujejo od 1% do 17% trehaloze v obliki suhe teže. Trehalozo najdemo tudi v mikroorganizmih, kot so pekovski in vinski kvas, kjer jo presnavlja veliko število bakterij, vključno s Streptococcus mutans, ki je ustna bakterija odgovorna za zobno gnilobo. Trehaloza je v mikobakterijah in korinebakterijah (rod Corynebacterium) integralna komponenta različnih glikolipidov, ki so pomembni za strukturo celične stene. Trehaloza zelo omeji škodo, ki bi nastala na proteinih, celicah, cepivih in raznih farmacevtskih oblikah pri postopkih shranjevanja in liofilizacije, zato se v takih procesih uporablja kot protektant.
Zaradi svoje stabilnosti (ne reagira s proteini in aminokislinami) je zaželeno sladilo, kljub dejstvu, da je njena sladkost več kot polovica manjša od sladkosti saharoze.
Encim trehalaza ali glikozidna hidrolaza je v manjših količinah prisoten pri večini ljudi. S tem, ko trehalozo cepi v dve molekuli glukoze, olajša njeno absorpcijo v črevesju.
Insekti (leteči) uporabljajo trehalozo kot glavni ogljikov hidrat, ki skladišči energijo. Ena izmed možnih razlag za to je, da se s cepitvijo dvojne glikozidne vezi, sprostita dve molekuli glukoze, ki se kot energijsko bogati molekuli porabita za let. Takšno sproščanje energije je učinkovitejše,saj se pri škrobu s cepitvijo glikozidne vezi sprosti le ena molekula glukoze.
Biosinteza[uredi | uredi kodo]
Do sedaj so znane najmanj tri različne poti biosinteze trehaloze. Najbolj znana in razširjena vključuje pretvorbo glukoze iz UDP-glukoze (ali GDP-glukoze) v glukozo 6-fosfat in trehalozo- 6-fosfat in UDP. To reakcijo katalizira trehalozna fosfat sintaza (TPS ali OtsA v bakteriji Escherichia coli). Organizmi, ki uporabljajo to pot sinteze, imajo trehalozno-P fosfatazo (TPP), ki pretvori trehalozo-P v prosto trehalozo.
Drugo pot sinteze, ki je znana v bakterijah vključuje intramolekularno preureditev maltoze (glukozil-α1,4-glukopiranozid) iz 1,4 vezi v 1,1 vez trehaloze. Ta reakcija je katalizirana z encimom trehalozna sintaza in daje prosto trehalozo kot začeten produkt.
Tretja pot sinteze vključuje kar nekaj različnih encimov, prvi od teh preuredi glukozo na reducirajočem koncu glikogenske verige iz α-1,4 vezi v α,α-1,1 vez trehaloze. Drugi encim nato sprosti trehalozo z glikogenske verige.
V gobah se nahaja trehalozna fosforilaza, ki katalizira fosforilacijo trehaloze v glukozo-1-fosfat in glukozo. Ta reakcija je reverzibilna in vitro in teoretično daje trehalozo iz glukoze-1-P in glukoze. Naslednji pomembni encim v metabolizmu trehaloze je trehalaza (T), ki naj bi bil vključen v energijski metabolizem in ima tudi regulatorno vlogo, s tem da kontrolira nivo glukoze v celici. Trehalaza naj bi bila pomembna v zmanjševanju koncentracije trehaloze. Zadnje študije na kvasovkah kažejo, da encimi, vključeni v sintezo trehaloze (TPS, TPP) obstajajo skupaj v kompleksu, ki je visoko reguliran.
Proizvodnja[uredi | uredi kodo]
Trehaloza je bila sprva pridobljena z ekstrakcijo iz kvasne kulture, ker pa so bili proizvodni stroški preveliki, je bila uporabljena le za določene kemikalije in kozmetiko.
Leta 1994 je družba Hayashibara, proizvajalec škroba v Okayami na Japonskem, odkrila poceni način masovne proizvodnje trehaloze iz škroba. Naslednje leto so proizvedli trehalozo z aktivacijo dveh encimov »encim, ki proizvaja glukoziltehalozo« spremeni reducirajoči konec škroba v trehalozno strukturo, »trehaloza sprostitveni encim« pa odklopi to trehalozno strukturo iz škroba. Kot rezultat dobimo iz škroba trehalozo visoke čistosti.
Uporaba[uredi | uredi kodo]
Trehaloza je bila sprejeta kot nova živilska sestavina v skladu s pogoji GRAS v ZDA in EU. Trehaloza je komercialno uporabljena kot sestavina živil. Je dober konzervans, saj ohranja kakovost treh glavnih skupin hranil (ogljikovi hidrati, beljakovine, maščobe) in je zmožna velikega zadrževanja vode, s tem pa ohranja teksturo hrane in jo ščiti pred izsušitvijo ali zamrzovanjem. Trehaloza ima tudi sposobnost prekrivanja grenkobe, ostrih okusov in vonja surove hrane in pakiranih živil. Taka kombinacija lastnosti privede do široke uporabe.
Tehnologija proizvodnje trehaloze je bila razvita na Japonskem, kjer z encimom spremenijo pšenični in koruzni sirup v trehalozo.
V raziskavah se trehaloza uporablja kot proteinski stabilizator in je zlasti učinkovita v kombinaciji s fosfatnimi ioni. Trehaloza je bila prav tako uporabljena v več biofarmacevtskih formulacijah monoklonskih protiteles: trastuzumab in bevacizumab, ki se tržita kot Herceptin in Avastin, (Genentech) in ranibizumab, ki se trži kot Lucentis (Genentech in Novartis).
V kozmetiki izkoriščajo sposobnost trehaloze, da zadržuje vodo in deluje kot vlažilec v mnogih produktih za osebno higieno, kot so kopalna olja in toniki za rast las.
V farmaciji izkoriščajo lastnost trehaloze, da deluje kot protektant proteinov in tkiv pri pripravi raztopin za prenos organov (pri presajanju organov).
Viri in literatura[uredi | uredi kodo]
- ↑ T. Novel functions and applications of trehalose. Pure Appl. Chem. 74(7):1263-1269. 2002.
- ↑ Lide, David R. (1998). Handbook of Chemistry and Physics (87 izd.). Boca Raton, FL: CRC Press. str. 3–534. ISBN 0849305942.
- Elbein AD, Pan YT, Pastuszak I, Carroll D. New insights on trehalose: a multifunctional molecule. Department of Biochemistry and Molecular Biology, University of Arkansas for Medical Sciences, Little Rock, AR 72205, USA. Review
- Schiraldi C, Di Lernia I, De Rosa M: Trehalose production: exploiting novel approaches. Trends Biotechnol. 2002 Oct; 20(10):420-5. Review
- Sawacx Murao, Hiroto Nagano, Sei Ogura and Toyokazu Nishino: Enzymatic Synthesis of Trehalose from Maltose, Department of Agricultural Chemistry, College of Agriculture
- T. Novel functions and applications of trehalose. Pure Appl. Chem. 74(7):1263-1269. 2002. Takanobu Higashiyama: Novel functions and applications of trehalose, Amase Institute of Hayashibara Biochemical Laboratory, Inc., 7-7 Amase Minami-Machi Okayama 700-0834, Japan
- spletni vir: http://www.answers.com/topic/trehalose
