Radikalska adicija
Radikalska adicija je organska adicijska reakcija, v kateri so udeleženi prosti radikali.[1] Predpogoj za potek reakcije je multipla (dvojna ali trojna) vez. Reakcija lahko poteče med radikalom in neradikalom ali med dvema radikaloma.
Reakcija poteka v treh osnovnih korakih, znanih tudi kot radikalni verižni mehanizem:
- Iniciacija (začetek reakcije oziroma nastanek radikalov), ki jo sproži radikalni iniciator: iz neradikalskega prekurzorja nastane prosti radikal.
- Propagacija (širitev reakcije oziroma verižna reakcija): radikal reagira z neradikalom, pri čemer nastane nov radikal.
- Terminacija (zaključek oziroma prekinitev reakcije): dva radikala reagirata drug z drugim, tako da nastane neradikal in nadaljevanje reakcije ni mogoče.
Radikalska reakcija je omejena na reagente z (relativno) šibko vezjo, ki s homolizo tvorijo proste radikale. Homolizo pogosto povzročita toplota in/ali svetloba. Reagenti z močnejšimi vezmi reagirajo z drugačnimi reakcijskimi mehanizmi.
Zančilni radikalski adiciji sta adiciji alkoholov in aldehidov na alkene, na primer metanola na eten, pri čemer nastane propanol:
- CH2=CH2 + CH3-OH → CH3-CH2-CH2-OH
in adicija acetaldehida na eten, pri čemer nastane butanon:
- CH2=CH2 + CH3-CHO → CH3-CH2-CO-CH3
Adicija bromovodika na alken[uredi | uredi kodo]
Radikalska adicija je tudi ne-Markovnikovova adicija bromovodika (HBr) na alken. Reakcijo katalizira, bolj natančno rečeno inicira, organski peroksid, ki iz HBr iztrga kisli proton, tako da nastane bromidni radikal Br•. Reakcija se prekine, ko se porabita ekvivalentni količini alkena in bromovodika.

Radikal se veže na bolj substituirani ogljikov atom. Radikalski adiciji HCl in HI ne potečeta, ker sta obe reakcij ekstremno endotermni.
Samoprekinjena oksidativna radikalska ciklizacija[uredi | uredi kodo]
Posebna vrsta radikalske adicije je samoprekinjena oksidativna radikalska ciklizacija, v kateri se alkini najprej oksidirajo v ketone, ketoni pa intramolekularno sklenejo obroč. Tovrstna reakcja se prekine sama od sebe, ker po sklenitvi obroča nadaljevanje reakcije ni mogoče. V reakciji se porabi stehiometrična količina iniciatorja.[2]
Eden od možnih iniciatorjev takšne radikalske adicije je nitratni radikal, ki nastane s fotolizo cerovega amonijevega nitrata (NH4)2[Ce(NO3)5]. Nitratni radikal reagira z alkinom, pri čemer najprej nastane zelo reaktiven vinilni radikal. S prenosom vodikovega atoma (1,5) pride do zapiranja obroča in tvorbe ketilnega radikala. Ketilni radikal nato odcepi nitritni radikal, ki pa ni dovolj reaktiven, da bi nadaljeval reakcijo. Reakcija se zato ustavi na stopnji ketona.
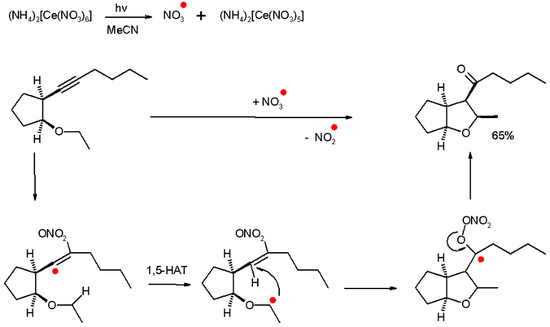
Učinkoviti radikali so enoatomni kisik (sinton), sulfatni radikalski ion SO4 iz amonijevega persulfata ((NH4)2S2O8) in hidroksilni radikal OH•.
Glej tudi[uredi | uredi kodo]
Viri in opombe[uredi | uredi kodo]
- ↑ L.G. Wade's Organic Chemistry 5th Ed. (p 319) - Mechanism supplements original.
- ↑ Self-Terminating, Oxidative Radical Cyclizations Tim Dreessen, Christian Jargstorff, Lars Lietzau, Christian Plath, Arne Stademann and Uta Wille, Molecules (journal)2004, 9, 480–497 Online article
