Peroksid
Videz
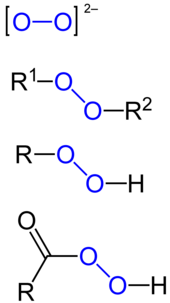
Peroksidi so skupina kemičnih spojin z osnovno zgradbo R−O−O−R, kjer sta molekuli kisika med seboj povezani s kovalentno vezjo, »R« pa je katerikoli element ali stranska veriga.[1][2] Skupini O−O v kemiji pravimo peroksidna ali peroksi skupina, včasih pa tudi perokso ali peroksilna skupina. Nomenklatura ni povsem dorečena.[3] Ime je leta 1804 skoval škotski kemik Thomas Thomson za opis oksidov z največjo količino kisika.[4]
Najobičajnejši peroksid je vodikov peroksid (H2O2), ki mu pogovorno pravimo kar »peroksid«. Pogosto se uporabljajo tudi razni organski peroksidi. Zaradi šibke kovalentne vezi med kisikovima atomoma so zelo reaktivni in dobri oksidanti.[5]
Sklici
[uredi | uredi kodo]- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. izd.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ Smith, Michael B.; March, Jerry (2007). Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6. izd.). New York: Wiley-Interscience. ISBN 978-0-471-72091-1.
- ↑ IUPAC, Compendium of Chemical Terminology, 2. izd. (the "Gold Book") (1997). Spletna izdaja: (2006–) "peroxides". DOI: 10.1351/goldbook.P04510
- ↑ Harper, Douglas. »peroxide«. Online Etymology Dictionary.
- ↑ Clark, Donald E. (september–oktober 2001). »Peroxides and peroxide-forming compounds« (PDF). Chemical Health & Safety. str. 13–22.
{{navedi revijo}}: Vzdrževanje CS1: samodejni prevod datuma (povezava)
