Hiperurikemija
| Hiperurikemija | |
|---|---|
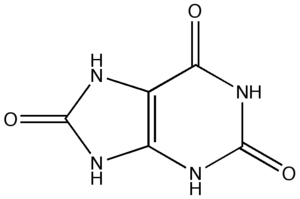 | |
| Sečna kislina | |
| Specialnost | endokrinologija |
| Klasifikacija in zunanji viri | |
| MKB-10 | E79.0 |
| MKB-9 | 790.6 |
| DiseasesDB | 5375 |
| eMedicine | med/1112 |
| MeSH | D033461 |
Hiperurikemija je nenormalno povišanje koncentracije sečne kisline v krvi. Pri človeku je zgornja mejna vrednost krvne koncentracije sečne kisline 360 µmol/L (6 mg/dL) za ženske in 400 µmol/L (6.8 mg/dL) za moške.[1]
Vzroki[uredi | uredi kodo]
Povišane ravni sečne kisline povzročajo različni dejavniki, vključno z genetskim nagnjenjem, odpornostjo proti insulinu, povišanim krvnim tlakom, oslabelim ledvičnim delovanjem, debelostjo, prehrano, uporabo diuretikov in uživanjem alkohola.[2] Med naštetimi je uživanje alkohola najpomembnejši vzrok.[3]
Vzroki hiperurikemije se lahko uvrstijo v tri skupine:[4] povišana proizvodnja sečne kisline, zmanjšano izločanje sečne kisline ter vzroki mešanega tipa. Povišano proizvodnjo lahko povzročita visoka vsebnost purinov v prehrani in povečana presnova purinov. Zmanjšano izločanje je lahko posledica ledvičnih obolenj, nekaterih zdravil ter kompeticija za ekskrecijo med sečno kislino in drugimi molekulami. Med vzroke mešanega tipa uvrščamo visoke koncentracije alkohola in/ali fruktoze v krvi ter stradanje.
Povišana proizvodnja[uredi | uredi kodo]
Hrana, bogata s purini, redko povzroči hiperurikemijo in sama ne more biti zadosten vzrok za njen pojav. Vsebnost purinov je v različnih vrstah hrane različna. Pri povzročanju povečane proizvodnje sečne kisline naj bi bila pomembnejša hrana, bogata s purinskima molekulama adeninom in hipoksantinom.[5]
Hiperurikemija zaradi povišane proizvodnje sečne kisline je pogost zaplet po presaditvi organov.[6] Sindrom tumorske lize lahko povzroči zelo visoke ravni sečne kisline v krvi, ki pogosto vodijo v ledvično odpoved. Tudi Lesch-Nyhanov sindrom povezujejo z zelo visokimi krvnimi koncentracijami uratov.
Zmanjšano izločanje[uredi | uredi kodo]
Hiperurikemijo zaradi zavrtega izločanja sečne kisline povzročajo predvsem zdravila iz skupine antiurikozurikov. Druga zdravila in snovi, ki delujejo na ta način, so še diuretiki, salicilati, pirazinamid, etambutol, nikotinska kislina, ciklosporin, 2-etilamino-1,3,4-tiadiazol ter citostatiki.[7]
Gen SLC2A9 nosi zapis za beljakovino, ki pomaga pri izplavljanju sečne kisline iz ledvic. Določeni polimorfizmi posameznega nukleotida pomembno vplivajo na krvne koncentracije sečne kisline.[8]
Ketogena dieta ovira zmožnost ledvic za izločanje sečne kisline zaradi kompeticije med sečno kislino in ketoni na prenašalnih beljakovinah.[9]
Na ledvično funkcijo in posledično hiperurikemijo pomembno vpliva tudi povišana krvna koncentracija svinca, vendar vzročna povezava ni pojasnjena.[10]
Vzroki mešanega tipa[uredi | uredi kodo]
V to skupino sodijo dejavniki, ki izkazujejo oboje delovanje, torej povišano proizvodnjo in zavrto izločanje sečne kisline.
Prekomerno uživanje alkohola je pomemben vzrok hiperurikemije. Proizvodnjo sečne kisline poviša s tem, da povzroči povišano nastajanje mlečne kisline in s tem laktično acidozo. Poviša tudi plazemsko koncentracijo hipoksantina in ksantina, ker pospeši presnovo adeninskih nukleotidov. Morda je tudi šibek zaviralec ksantinske dehidrogenaze. Nadalje, pivo vsebuje zaradi fermentacije purine. Etanol znižuje izločanje sečne kisline skozi ledvice, ker povzroča dehidracijo in v redkih primerih tudi ketoacidozo.[3]
Hrana z visoko vsebnostjo fruktoze znatno doprinese k tveganju za hiperurikemijo.[11][12][13] Povišane vrednosti sečne kisline so posledica produkta presnove fruktoze, ki deluje na presnovo purinov. Pride do povečane pretvorbe ATP-ja v inozin in posledično v sečno kislino ter do povečane sinteze purinov.[14] Hkrati pa fruktoza tudi zavira izločanje sečne kisline zaradi kompeticije na prenašalni beljakovini SLC2A9.[15] Učinek fruktoze na izločanje sečne kisline je izrazitejši pri posameznikih z dednim nagnjenjem za hiperurikemijo in putiko.[14]
Pri stradanju začne telo presnavljati lastna tkiva, ki pa so bogata s purini. Tako pride, podobno kot pri s purini bogati prehrani, do povečane pretvorbe purinov v sečno kislino. Pri zelo nizko kalorični prehrani brez ogljikovih hidratov lahko nastopi zelo huda hiperurikemija.[16] Stradanje tudi moti izločanje sečne kisline zaradi kompeticije s ketoni.[17]
Zdravljenje[uredi | uredi kodo]
Obarjanje kristalov sečne kisline in obratno tudi njihovo raztapljanje sta odvisna od koncentracije sečne kisline, pH-ja, koncentracije natrija in temperature. Zdravljenje temelji na teh parametrih.
Koncentracija[uredi | uredi kodo]
Po Le Chatelierevem načelu znažanje koncentracije sečne kisline v krvi povzroči raztapljanje kristalov v kri, iz katere se nato izloča skozi ledvice. Vzdrževanje nizke koncentracije sečne kisline preprečuje nadaljnje obarjanje novih kristalov. Če ima bolnik kronični protin (putiko) ali uratne tofe, lahko pride do obsežnega nalaganja uratnih kristalov v sklepih in drugih tkivih in v takih primerih je po navadi potrebno agresivno in dolgotrajno zdravljenje.
Najpogosteje uporabljana zdravila pri hiperurikemiji so dveh vrst: zaviralci ksantinske oksidaze in urikozuriki. Prvi znižajo proizvodnjo sečne kisline, tako da vplivajo na encim ksantinsko oksidazo, drugi pa povečajo izločanje sečne kisline skozi ledvice, saj zavrejo reabsorpcijo sečne kisline nazaj v kri. Pri bolnikih, ki so na hemodializi, lahko sevelamer znatno zmanjša krvne vrednosti sečne kisline,[18][19] in sicer z adsorpcijo uratov v črevesju.[19] Pri ženskah povezujejo kombinirane peroralne kontraceptive z znatnim znižanjem serumskih koncentracij sečne kisline.[20]
Nemedikamentozno zdravljenje hiperurikemije vključuje dieto z nizko vsebnostjo purinov ter različna prehranska dopolnila. Vendar številni zdravniki menijo, da je omenjeni način zdravljena le malo učinkovit oziroma sploh neučinkovit. Uporabljale so se tudi litijeve soli, saj litij poveča topnost uratov.
pH[uredi | uredi kodo]
Spreminjanje serumskega pH-ja ni ne enostavno ne varno. Zdravljenje na načelu spreminjanja pH-ja temelji zlasti na spreminjanju kislosti seča, s čimer se zmanjša tveganje za nastanek ledvičnih uratnih kamnov. Sredstva, ki lahko pomagajo pri naalkaljenju seča, so natrijev bikarnonat, kalijev citrat, magnezijev citrat in Shohlova raztopina (ki jo sedaj nadomeščajo z Bicitro[21]). Zdravilo s podobnim učinkom je acetazolamid.
Temperatura[uredi | uredi kodo]
Nizka temperatura je sprožilni dejavnik akutnega napada putike, kar je najverjetneje posledica odvisnosti obarjanje kristalov sečne kisline v tkivih pri nižjih temperaturah. Tako je eden od ukrepov preprečevanja napadov putike vzdrževanje okončin toplih; pomaga lahko tudi namakanje v topli vodi.
Prognoza[uredi | uredi kodo]
Hiperurikemija lahko vodi v putiko in pri močnem povišanju koncentracij sečne kisline tudi do ledvične odpovedi.
Viri[uredi | uredi kodo]
- ↑ Chizyński K; Rózycka M (2005). »Hyperuricemia«. Pol. Merkur. Lekarski (v poljščini). 19 (113): 693–696. PMID 16498814.
- ↑ Sun, Sam Z.; Flickinger, Brent D.; Williamson-Hughes, Patricia S.; Empie, Mark W. (Marec 2010). »Lack of association between dietary fructose and hyperuricemia risk in adults«. Nutrition & Metabolism. 7 (16). doi:10.1186/1743-7075-7-16.
- ↑ 3,0 3,1 Yamamoto T; Moriwaki Y; Takahashi S (Junij 2005). »Effect of ethanol on metabolism of purine bases (hypoxanthine, xanthine, and uric acid)«. Clinica Chimica Acta; International Journal of Clinical Chemistry. 356 (1–2): 35–57. doi:10.1016/j.cccn.2005.01.024. PMID 15936302.
- ↑ Yamamoto T (april 2008). »[Definition and classification of hyperuricemia]«. Nippon Rinsho (v japonščini). 66 (4): 636–640. PMID 18409507.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Brulé D; Sarwar G; Savoie L (1992). »Changes in serum and urinary uric acid levels in normal human subjects fed purine-rich foods containing different amounts of adenine and hypoxanthine«. J Am Coll Nutr. 11 (3): 353–358. PMID 1619189.
- ↑ Stamp L; Searle M; O'Donnell J; Chapman P (2005). »Gout in solid organ transplantation: a challenging clinical problem«. Drugs. 65 (18): 2593–2611. PMID 16392875.
- ↑ Scott JT (april 1991). »Drug-induced gout«. Baillieres Clin Rheumatol. 5 (1): 39–60. doi:10.1016/S0950-3579(05)80295-X. PMID 2070427.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Brandstätter A; Kiechl S; Kollerits B; Hunt SC; Heid IM; Coassin S; Willeit J; Adams TD; Illig T; Hopkins PN; Kronenberg F (Avgust 2008). »Sex-specific association of the putative fructose transporter SLC2A9 variants with uric acid levels is modified by BMI«. Diabetes Care. 31 (8): 1662–1667. doi:10.2337/dc08-0349. PMC 2494626. PMID 18487473.
- ↑ Förster H (Avgust 1979). »[Possibilities for weight reduction by means of diet]«. Fortschr. Med. (v nemščini). 97 (32): 1339–1344. PMID 488876.
- ↑ Lai LH; Chou SY; Wu FY; Chen JJ; Kuo HW (Avgust 2008). »Renal dysfunction and hyperuricemia with low blood lead levels and ethnicity in community-based study«. Sci. Total Environ. 401 (1–3): 39–43. doi:10.1016/j.scitotenv.2008.04.004. PMID 18514766.
- ↑ Nakagawa T; Hu H; Zharikov S; in sod. (2006). »A causal role for uric acid in fructose-induced metabolic syndrome«. Am. J. Physiol. Renal Physiol. 290 (3): F625–631. doi:10.1152/ajprenal.00140.2005. PMID 16234313.
- ↑ Mayes PA (1993). »Intermediary metabolism of fructose«. Am. J. Clin. Nutr. 58 (5 Suppl): 754S–765S. PMID 8213607.
- ↑ Miller A; Adeli K (Marec 2008). »Dietary fructose and the metabolic syndrome«. Curr. Opin. Gastroenterol. 24 (2): 204–9. doi:10.1097/MOG.0b013e3282f3f4c4. PMID 18301272.
- ↑ 14,0 14,1 Mayes PA (november 1993). »Intermediary metabolism of fructose«. Am. J. Clin. Nutr. 58 (5 Suppl): 754S–765S. PMID 8213607.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Vitart V; Rudan I; Hayward C; Gray NK; Floyd J; in sod. (april 2008). »SLC2A9 is a newly identified urate transporter influencing serum urate concentration, urate excretion and gout«. Nat. Genet. 40 (4): 437–442. doi:10.1038/ng.106. PMID 18327257.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Howard AN (1981). »The historical development, efficacy and safety of very-low-calorie diets«. Int J Obes. 5 (3): 195–208. PMID 7024153.
- ↑ Kirch W; von Gicycki C (april 1980). »[Renal function in therapeutic starvation (author's transl)]«. Wien. Klin. Wochenschr. (v nemščini). 92 (8): 263–266. PMID 7405247.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Garg JP; Chasan-Taber S; Blair A; in sod. (Januar 2005). »Effects of sevelamer and calcium-based phosphate binders on uric acid concentrations in patients undergoing hemodialysis: a randomized clinical trial«. Arthritis and rheumatism. 52 (1): 290–295. doi:10.1002/art.20781. PMID 15641045.
- ↑ 19,0 19,1 Ohno I; Yamaguchi Y; Saikawa H; Uetake D; Hikita M; Okabe H; Ichida K; Hosoya T (2009). »Sevelamer decreases serum uric acid concentration through adsorption of uric acid in maintenance hemodialysis patients«. Internal Medicine (Tokyo, Japan). 48 (6): 415–420. PMID 19293539.
- ↑ Gresser U; Gathof B; Zöllner N (december 1990). »Uric acid levels in southern Germany in 1989. A comparison with studies from 1962, 1971, and 1984«. Klin. Wochenschr. 68 (24): 1222–1228. PMID 2290309.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Ross, Mary. Rx Update December 1993. University of Iowa. 16. 2. 2009. URL:http://www.healthcare.uiowa.edu/pharmacy/RxUpdate/1993/12.December.html Arhivirano 2008-10-19 na Wayback Machine.. Vpogled: 16. 2. 2009. (Archived by WebCite at)
