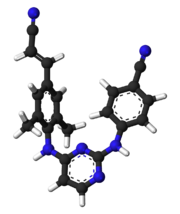
Rilpivirin
 | |
 | |
| Klinični podatki | |
|---|---|
| Blagovne znamke | Edurant |
| AHFS/Drugs.com | Consumer Drug Information |
| MedlinePlus | a611037 |
| Licenčni podatki |
|
| Nosečnostna kategorija |
|
| Način uporabe | peroralno |
| Oznaka ATC | |
| Pravni status | |
| Pravni status |
|
| Farmakokinetični podatki | |
| Razpolovni čas | 38 ur |
| Identifikatorji | |
| |
| Številka CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| ChEMBL | |
| NIAID ChemDB | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.224.394 |
| Kemični in fizikalni podatki | |
| Formula | C22H18N6 |
| Mol. masa | 366,42 g/mol |
| |
Rilpivirin (TMC278, zaščiteno ime Edurant) je zdravilo za zdravljenje okužbe z virusom HIV.[1][2] Spada v skupino nenukleozidnih zaviralcev reverzne transkriptaze (NNRTI) druge generacije z višjo potentnostjo, daljšim razpolovnim časom in ugodnejšim profilom neželenih učinkov kot starejši NNRTI-ji, npr. efavirenz.[3][4]
Zgodovina[uredi | uredi kodo]
Rilpivirin je vstopil v klinične študije faze III aprila 2008,[5][6] maja 2011 pa je pridobil dovoljenje za promet v ZDA.[7] Zdravilo s kombinacijo fiksnih odmerkov rilpivirina ter emtricitabina in tenofovirja pod zaščitenim imenom Complera je ameriški Urad za prehrano in zdravila odobril avgusta 2011.[8] Pod zaščitenim imenom Eviplera je bilo to zdravilo odobreno v državah Evropske zveze novembra 2011.[9]
Neželeni učinki[uredi | uredi kodo]
Najpogostejši neželeni učinki, ki se pojavijo pri več kot 1 na 10 bolnikov, so povečana koncentracija holesterola in LDL (lipoprotein majhne gostote) v krvi pri zaužitju na tešče, glavobol in povišane vrednosti aminotransferaz.[10]
Viri[uredi | uredi kodo]
- ↑ »TMC278 - A new NNRTI«. Tibotec. Arhivirano iz prvotnega spletišča dne 20. decembra 2008. Pridobljeno 7. marca 2010.
- ↑ Stellbrink HJ (2007). »Antiviral drugs in the treatment of AIDS: what is in the pipeline ?«. Eur. J. Med. Res. 12 (9): 483–495. PMID 17933730.
- ↑ Goebel F; Yakovlev A; Pozniak AL; Vinogradova E; Boogaerts G; Hoetelmans R; de Béthune MP; Peeters M; Woodfall B (2006). »Short-term antiviral activity of TMC278--a novel NNRTI--in treatment-naive HIV-1-infected subjects«. AIDS. 20 (13): 1721–1726. doi:10.1097/01.aids.0000242818.65215.bd. PMID 16931936.
- ↑ Pozniak A, Morales-Ramirez J, Mohap L et al. 48-Week Primary Analysis of Trial TMC278-C204: TMC278 Demonstrates Potent and Sustained Efficacy in ART-naïve Patients. Arhivirano 2007-10-19 na Wayback Machine. Oral abstract 144LB.
- ↑ ClinicalTrials.gov A Clinical Trial in Treatment naïve HIV-1 Patients Comparing TMC278 to Efavirenz in Combination With Tenofovir + Emtricitabine
- ↑ ClinicalTrials.gov A Clinical Trial in Treatment naïve HIV-Subjects Patients Comparing TMC278 to Efavirenz in Combination With 2 Nucleoside/Nucleotide Reverse Transcriptase Inhibitors
- ↑ »FDA approves new HIV treatment«. FDA. Pridobljeno 20. maja 2011.
- ↑ »Approval of Complera: emtricitabine/rilpivirine/tenofovir DF fixed dose combination«. FDA. 10. avgust 2011.
- ↑ http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/002312/human_med_001514.jsp&mid=WC0b01ac058001d124 Arhivirano 2013-05-24 na Wayback Machine., vpogled: 5. 3. 2012.
- ↑ http://www.ema.europa.eu/docs/sl_SI/document_library/EPAR_-_Product_Information/human/002264/WC500118874.pdf Arhivirano 2012-05-17 na Wayback Machine., Povzetek glavnih značilnosti zdravila Edurant, vpogled: 5. 3. 2012.
