Diboran
| Članek potrebuje lekturo pravopisa, vrstnega reda besed, tona ali sloga. (mesec ni naveden) |

| |

| |
| Imena | |
|---|---|
| IUPAC ime
Diboran(6)
| |
| Identifikatorji | |
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.039.021 |
| EC število |
|
| RTECS število |
|
CompTox Dashboard (EPA)
|
|
| |
| |
| Lastnosti | |
| B2H6 | |
| Molska masa | 27,67 g·mol−1 |
| Videz | Brezbarvni plin |
| Gostota | 1.216 g/dm3 |
| Tališče | −16.485 °C (−29.641 °F; −16.212 K) |
| Vrelišče | −925 °C (−1.633 °F; −652 K) |
| Struktura | |
| Koordinacijska geometrija |
Tetraednična (za boron) |
| Oblika molekule | see text |
| Dipolni moment | 0 D |
| Nevarnosti | |
| NFPA 704 (diamant ognja) | |
| Sorodne snovi | |
| Sorodno boron compounds | Dekaboran BF3 |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Diboran je kemična spojina sestavljena iz bora in vodika s formulo B2H6. To je brezbarven plin, ki ima pri sobni temperaturi odbijajoče sladek vonj. Diboran med mešanjem z zrakom, lahko tvori eksplozivne zmesi. V vlažnem zraku pri sobni temperaturi pa se zlahka vname. Sinonimi so boroethane, borov hidrid, in diborovega hexahydrida. Diboran je ključna borova spojina iz različnih aplikacij. Razvrščamo ga med "endotermna", kar pomeni, da je njegova toplota nastajana, pozitivna. Kljub termodinamični nestabilnosti, je diboran kinetično robusten in razstavlja veliko kemije, veliko od tega pa posledično izgubi vodik.
Struktura[uredi | uredi kodo]
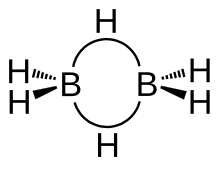
V zaobljeni liniji prikazuje dva elektrona obveznic, ki sta sestavljena iz treh atomov vodika, dva bora lepljenih atomov in atom v sredini. Diboran sprejme D2H strukturo, ki vsebuje štiri terminalna in dva premostitvena atoma vodika. Model molekulskih orbital kaže, da so vezi bora in terminalov atoma vodika konvencionalne v dveh centrih in dveh elektronov kovalentne vezi. Vezi med atomi bora in premostitvenih vodikovih atomov pa so drugačni od molekule, kot so ogljikovodiki. Uporabljajo dva elektrona v vezi s terminali vodikovih atomov, vsak bor ima eno valentni elektron ki ostane za dodatno lepljenje. Premostitveni vodikovi atomi zagotovijo po en elektron vsak. Tako je B2H2 obroč, ki drži skupaj štiri elektrone, na primer tri centre in dva elektrona za lepljenje. Ta vrsta vezi se včasih imenuje "banana vez". Dolžine obveznic B-H mostu in B-H terminala so 1,33 in 1,19 Å. Ta razlika v dolžini teh obveznic odraža razlike v njihovi moči, za B-H mostove je relativno šibka. Struktura je isoelectronic zC2H62+, ki izhajale iz diprotona in molekule etena. [1] Diboran je eden od mnogih spojin s tako nenavadno vezjo. [2]
Proizvodnja in sinteza[uredi | uredi kodo]
Diboran je pomemben, preučevali so ga tako pogosto, da obstaja veliko sintez. Večina priprav je posledica reakcije hidrida darovalcev z borom halogenidov. Industrijska sinteza vključuje zmanjšanje BF z natrijevim hidridom:
2 BF3 + 6 NaH → B2H6 + 6 NaF
Dve laboratorijski metodi začeti od bor triklorida z litijem aluminijevega hidrida ali borovega trifluorida so rešene, z borohidrid natrijem. Obe metodi doprineseta do 30% diborane:
4 BCl3 + 3 LiAlH4 → 2 B2H6 + 3 LiAlCl4
4 BF3 + 3 NaBH4 → 2 B2H6 + 3 NaBF4
S Starejšimi metodami pa neposredno reakcijo borohydrid soli z oksidacijsko kislino (npr.fosforna kislino) ali z razredčenjem žveplove kisline:
2 BH4− + 2 H+ → 2 H2 + B2H6
Podobno se je oksidacija borohydrid soli pokazala in je še vedno primerna za manjše priprave lestvice. Na primer, z uporabo joda kot oksidant.
Reakcija[uredi | uredi kodo]
Diboran je zelo reaktiven in vsestranski reagent. Njegova reakcija dominira, vzorec pa vključuje oblikovanje aduktov z bazami Lewis. Reagira z amoniakom ali diammoniate iz diborana, odvisno od uporabljenih pogojev. Diboran tudi hitro reagira z alken izdelki. Diborane reagira z vodo v obliki vodika in borove kisline. Ter je spojina kompleksne oblike z Lewis bazo. Opazni so kompleksi s THF in dimetil sulfidom, tako tekoče spojine, ki so priljubljeni reducenti v organski kemiji.
Diboran reagira z vodo, da oblikuje vodik in borovo kislino: B2H6 + 6 H2O › 2 B(OH)3 + 6 H2 Diboran reagira z metanolom, kar da vodik and trimetoksiborov ester: B2H6 + 6 MeOH › 2 B(OMe)3 + 6 H2 Diboran z natrijevim amalgamom da NaBH4 in Na[B3H8]. Ko diboranu dodamo litijev hidrid in dietil eter, nastane Litijev borohidrid: B2H6 + 2 LiH › 2 LiBH4 Diboran reagira z brezvodnim vodikovim kloridom ali plinom vodikovim bromidom, ki da bor halohidrid: B2H6 + HX › B2H5X + H2 (X = Cl, Br) Diboran reagira z ogljikovim monoksidom pri 470 K in 20 barih, kar da H3BCO.
Druga raba[uredi | uredi kodo]
Diboran se uporablja kot raketno gorivo, kot gume v vulkanizerstvu, kot katalizator za ogljikovodik v polimerizaciji, kot plamen-hitrost plin, in kot doping sredstvo za proizvodnjo polprevodnikov. Prav tako je v vmesni proizvodnji visoko čistega bora za proizvodnjo polprevodnikov. Prav tako ga uporabljajo kot premaz za stene ter za zmanjševanje vsebnosti težkih kovin in nečistoč v plazmi.
Varnost[uredi | uredi kodo]
Toksičen učinek diborana je draženje, predvsem zaradi svojih lastnosti. Kratkotrajna izpostavljenost diboranu lahko povzroči občutek tiščanja v prsih, kratka sapa, kašelj in sopenje. Ti znaki in simptomi se lahko pojavijo takoj ali z zamikom do 24 ur. Lahko se pojavi razdražena koža in oči. Študije so pokazale, da diboran povzroča isto vrsto učinkov na živalih, kot opaženih pri ljudeh.
Ljudje, ki so dalj časa izpostavljeni nizkim količinam diborana, so že doživeli draženje dihal, napade, utrujenost, zaspanost, zmedenost, tresenje...
Zgodovina[uredi | uredi kodo]
Diborane je bil prvič sintetizirali v 19. stoletju s hidrolizo kovinskih boridov, vendar ni bil nikoli analizirali. Od leta 1912 do 1936 je velik pionir v kemiji Alfred Stock svoje raziskave pripeljal do metode za sintezo in ravnanju z njimi zelo reaktivne, nestabilne in pogosto strupeno borovega hidride. Predlagal je podobno strukturo meritve diborana kot etanola. Bauerju se je sprva zdelo, da podprejo njegovo predlagano strukturo in fizikalne lastnosti borovega hidrida in njihovih derivatov.Zaradi osebne komunikacije z L. Pauling (ki so podprli etan podobno strukturo)in Schlessinger niso posebej razpravljali. S tremi jedri in dvemi elektronskimi vezmi v njegovem takrat klasičnem pregledu. Vendar pregled pove da razprava o C2 v strukturi pove globlji pomen "treba je priznati, da ta formulacija lahko predstavlja veliko kemičnih lastnosti diborana.Leta 1943 dodiplomski študent na Balliol College, Oxford, H. Christopher Longuet-Higgins, objavila trenutno sprejeto strukturo skupaj z RP Bell. Ta struktura je bila že opisana leta 1921. Po predlogu Longuet-Higgins/Bell priča pestro razpravo o pravilni strukturi. Razprava se je končala z elektronskim merjenjem difrakcijske leta 1951 Hedberg K. in V. Schomaker s potrditvijo strukture, prikazane v shemah na tej strani.
William Nunn Lipscomb še potrdili z molekularno strukturo boranes z uporabo X-ray kristalografije v 1950 in razvite teorije, da pojasni svoje trditve. Kasneje je uporabljal iste metode na povezanih težavah, vključno s strukturo Karborani, na katerega je usmerjena v raziskave v prihodnosti Nobelove nagrajenke Roald Hoffmann. Lipscombje prejel Nobelovo nagrado za kemijo leta 1976.Drugi Diboran je predlagal kot raketnega goriva in eksperimentalno odpustili, vendar se ne uporabljajo v vse za raketne storitev, kot vulcaniser gume, kot katalizator polimerizacije ogljikovodikov, kot plamen hitrosti plin, in kot doping sredstvo za proizvodnjo polprevodnikov . Prav tako vmesna v proizvodnji visoko čistega bora za proizvodnjo polprevodnikov. Uporablja se tudi za nanos stene tokamaki zmanjšati količino težkih kovin nečistoč v plazmi.
Varnost[uredi | uredi kodo]
Strupenost diborana so predvsem zaradi svojih dražilnih lastnosti. Kratkotrajna izpostavljenost diboranu lahko povzroči občutek tiščanja v prsih, težko dihanje, kašelj in piskanje. Ti znaki in simptomi se lahko pojavijo takoj ali z zamikom do 24 ur. Draženje kože in oči se lahko pojavijo tudi potem. Študije na živalih so pokazale, da povzroča diboran isto vrsto učinkov, opaženih pri ljudeh.
Ljudje, ki so izpostavljeni dalj časa v nizkih zneskih diboranu so doživeli draženje dihalnih poti, krči, utrujenost, zaspanost, zmedenost, tresenje ,itd.
Viri[uredi | uredi kodo]
- ↑ G. Rasul; G.K.S. Prakash; G.A. Olah (2005). »Comparative ab Initio Study of the Structures and Stabilities of the Ethane Dication C2H62+ and Its Silicon Analogues Si2H62+ and CSiH62+«. J. Phys. Chem. A. 109 (5): 798–801. doi:10.1021/jp0404652. PMID 16838949.
- ↑ Laslo P (2000). »A Diborane Story«. Angewandte Chemie International Edition. 39 (12): 2071–2072. doi:10.1002/1521-3773(20000616)39:12<2071::AID-ANIE2071>3.0.CO;2-C. PMID 10941018. abstract[mrtva povezava]

