Hidroksamska kislina
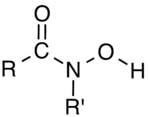
Hidroksamska kislina je skupina organskih spojin s funkcionalno skupino RC(O)N(OH)R', kjer sta R in R' organska dela, CO pa karbonilna skupina. Gre za amide (RC(O)NHR'), pri katerih je dušikov center NH substituiran s hidroksilno skupino OH. Pogosto se uporablja kot kelator kovin.
Sinteza in reakcije[uredi | uredi kodo]
Hidroksamske kisline se običajno pridobivajo bodisi iz estrov bodisi iz kislinskih kloridov z reakcijo s hidroksilaminskimi solmi. Za sintezo benzohidroksamske kisline je celokupna reakcija:[1]
- C6H5CO2Mi + NH2OH → C6H5C(O)NHOH + MeOH
Hidroksamske kisline se lahko sintetizirajo tudi iz aldehidov preko reakcije Angeli-Rimini.
Znana reakcija s hidroksamsko kislino je npr. Lossenova premestitev.
Koordinacijska kemija in biokemija[uredi | uredi kodo]
- Primeri spojin
-
Ferikrom
-
Deferoksamin
-
Rodotorulna kislina
Na področju koordinacijske kemije so hidroksamske kisline odlični ligandi.[2] Lahko oddajo vodikov atom, s čimer nastanejo hidroksamati, ki se vežejo na kovinske ione kot bidentatni ligandi. Afiniteta hidroksamatov do feri ionov je tako velika, da je narava razvila družine hidroksamskih kislin, ki delujejo kot železo vezoče spojine (siderofori) pri bakterijah, ki raztopijo netopne železove(III) spojine. Nastali železovi kompleksi se nato transportirajo v celice, kjer se železov ion odcepi in uporabi za metabolne reakcije.[3]
Ligandi, pridobljeni iz hidroksamske kisline in tiohidroksamske kisline, prav tako tvorijo močne komplekse s svincem(II).[4]
Druge uporabe in pojavljanja[uredi | uredi kodo]
Hidroksamske kisline se pogosto uporabljajo v flotaciji redkih zemljskih mineralov med koncentracijo ekstrakcijo rud za nadaljnjo obdelavo.
Nekatere hidroksamske kisline (npr. vorinostat, belinostat, panobinostat in trikostatin A) so inhibitorji HDAC s protirakavimi lastnostmi. Fosmidomicin je naravna hidroksamska kislina in zaviralec 1-deoksi-D-ksiluloza-5-fosfat reduktoizomeraze (DXP reduktoizomeraza). Hidroksamske kisline se tudi raziskujejo za predelavo obsevanega goriva.
Reference[uredi | uredi kodo]
- ↑ C. R. Hauser and W. B. Renfrow, Jr "Benzohydroxamic Acid" Org. Synth. 1939, volume 19, p. 15ff.
- ↑ Agrawal, Y K (1979). »Hydroxamic Acids and Their Metal Complexes«. Russian Chemical Reviews. Zv. 48, št. 10. str. 948. doi:10.1070/RC1979v048n10ABEH002422.
- ↑ Miller, Marvin J. (november 1989). »Syntheses and Therapeutic Potential of Hydroxamic Acid Based Siderophores and Analogues«. Chemical Reviews. Zv. 89, št. 7. str. 1563–1579. doi:10.1021/cr00097a011.
{{navedi revijo}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Farkas, Etelka; Buglyó, Péter (2017). »Chapter 8. Lead(II) Complexes of Amino Acids, Peptides, and Other Related Ligands of Biological Interest«. V Astrid, S. (ur.). Lead: Its Effects on Environment and Health. Metal Ions in Life Sciences. Zv. 17. de Gruyter. str. 201–240. doi:10.1515/9783110434330-008.


