Heksakloroetan

| |
| |
| Imena | |
|---|---|
| Priporočeno IUPAC ime
heksakloroetan | |
| Druga imena
ogljikov heksaklorid, etanov heksaklorid, perkloroetan
| |
| Identifikatorji | |
3D model (JSmol)
|
|
| 1740341 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.000.606 |
| EC število |
|
| Gmelin | 26648 |
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Lastnosti | |
| C2Cl6 | |
| Molska masa | 236,74 g/mol |
| Videz | brezbarvni kristali[1] |
| Vonj | podoben vonju kafre [1] |
| Gostota | 2,091 g/mL at 25 °C |
| Tališče | sublimira |
| Vrelišče | 183 °C (361 °F; 456 K) |
| 0,005% (22.2 °C)[1] | |
| Parni tlak | 0,2 mmHg (20 °C)[1] |
| Magnetna občutljivost | -112,7·10−6 cm3/mol |
| Nevarnosti | |
| Glavne nevarnosti | verjetno rakotvoren, nevaren zaviralec centralnega živčnega sistema |
| NFPA 704 (diamant ognja) | |
| Plamenišče | ni vnetljiv[1] |
| Smrtni odmerek ali koncentracija (LD, LC): | |
LD50 (srednji odmerek)
|
4460 mg/kg (podgana, oralno) 4970 mg/kg (morski prašiček, oralno) |
| NIOSH (ZDA varnostne meje): | |
PEL (Dopustno)
|
TWA 1 ppm (10 mg/m3) [koža][1] |
REL (Priporočeno)
|
Ca TWA 1 ppm (10 mg/m3) [koža][1] |
IDLH (Takojšnja nevarnost)
|
Ca [300 ppm][1] |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
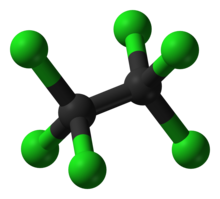
Heksakloroetan ali perkloroetan je organska klorova spojina s formulo (CCl3)2. Pri sobni temperaturi je bela brezbarvna trdnina s kafri podobnim vonjem.[3] Vojska ga je uporabljala v dimnih sestavkih na primer v dimnih granatah.
Pridobivanje
[uredi | uredi kodo]Najpogosteje uporabljen komercialni postopek za pridobivanje heksakloroetana je kloriranje tetrakloroetena pri 100–140 °C v prisotnosti železovega(III) klorida (FeCl3),
- Cl2C=CCl2 + Cl2 → Cl3C−CCl3
vendar obstaja tudi več drugih postopkov. Zelo čist heksakloroetan v majhnih količinaj je mogoče proizvesti s kloriranjem barijevega karbida.[4]:101 Proizvaja se tudi kot stranski proizvod industrijskega kloriranja drugih surovin.[4]:101
Uporaba
[uredi | uredi kodo]Heksakloroetan se je uporabljal v proizvodnji maziv za ekstremne tlake in sredstvo za prenos verige pri emulzijski polimerizaciji kopolimera propilen tetrafluoroeten. Heksakloroetan se uporablja kot sredstvo za odstranjevanje parazitov v veterinarski medicini, pospeševalnik vulkanizacije kavčuka, sestavina fungicidnih in insekticidnih preparatov, odganjalo moljev in mehčalo za celulozne estre.[3]
Heksakloroetan se je uporabljal tudi v proizvovodnji peletov za razplinjevanje mehurčkov vodika iz taline aluminija v livarnah aluminija. Na podoben način se uporablja pri ulivanju magnezija, vendar se njegova raba v livarnah v Evropski uniji postopoma opušča.[5]
Dimni plin
[uredi | uredi kodo]Heksakloroetanski dimni plin (HC) v dimnih granatah vsebuje približno enaki količini heksakloroetana in cinkovega oksida (ZnO) in približno 6% granuliranega aluminija. Tovrsten dimni plin je strupen zaradi tvorbe cinkovega klorida.[6][7] Tovrstne granate je zaradi strupenosti opustila večina armad zahodnih držav.[8]
HC se uporablja tudi za obvladovanje uličnih nemirov. Izpostavljenost tovrstnemu dimnemu plinu povzroča bruhanje in izgubo apetita in motnje v menstrualnem ciklu, vendar se še naprej uporablja. Laboratorij za biomedicinske raziskave in razvoj v vojski ZDA je ugotovil tudi to, da je "nekaj minutna izpostavljenost nezaščitenih vojakov visokim koncentracijam HC dima povzročila poškodbe in smrt."[9]
Toksičnost
[uredi | uredi kodo]Heksakloroetan ni posebej strupen, če se ga zaužije,[10] pri absorbciji skozi kožo pa velja za zelo strupenega. Primarni učinek heksakloroetana je depresija osrednjega živčevja.[3] Koncentracija v zraku, ki je takoj nevarna za življenje ali zdravje, je 300 ppm, dovoljena meja izpostavljenosti v skladu s predpisi za varstvo pri delu pa je 1 ppm (koža).[10] Upravičeno se domneva, da je rakotvoren.[11]
Sklici
[uredi | uredi kodo]- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 NIOSH Pocket Guide to Chemical Hazards. »#0316«. National Institute for Occupational Safety and Health (NIOSH).
- ↑ »Hexachloroethane«. Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ↑ 3,0 3,1 3,2 Snedecor, Gayle (1999). »Hexachloroethane«. V Kroschwitz, Jacqueline I. (ur.). Kirk-Othmer Concise Encyclopedia of Chemical Technology (4th izd.). New York: John Wiley & Sons, Inc. str. 428. ISBN 978-0471419617.
- ↑ 4,0 4,1 »Hexachloroethane 101« (PDF). september 1997.
{{navedi splet}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ ECHA, Annex XVII to REACH – Conditions of restriction, Restrictions on the manufacture, placing on the market and use of certain dangerous substances, mixtures and articles, entry 41: hexachloroethane
- ↑ »Appendix E: Smoke And Masking Agents« (PDF). Australian Department of Veteran Affairs. december 2003. str. E-3. Arhivirano iz prvotnega spletišča (PDF) dne 13. februarja 2014. Pridobljeno 4. oktobra 2012.
{{navedi splet}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ National Research Council (1997). Toxicity of Military Smokes and Obscurants, volume 1. Subcommittee on Military Smokes and Obscurants. Washington, DC: National Academy Press. p. 127
- ↑ Steinritz, D., Zehfuß, F., Stenger, B., Schmidt, A., Popp, T., Kehe, K., Mückter, H., Thiermann, H., Gudermann, T. (2018). Zinc chloride-induced TRPA1 activation does not contribute to toxicity in vitro. Toxicology Letters, 293, 133–139. doi:10.1016/j.toxlet.2017.09.008
- ↑ Lerner, Sharon (10. oktober 2020). »Toxic Chemical Smoke Grenades Used in Portland«. The Intercept (v angleščini). Pridobljeno 16. junija 2021.
- ↑ 10,0 10,1 »Documentation for Immediately Dangerous To Life or Health Concentrations (IDLHs) Hexachloroethane«. NIOSH. Maj 1994. Pridobljeno 4. oktobra 2012.
- ↑ »Report on Carcinogens, Twelfth Edition, Hexachloroethane« (PDF). NIH. 2011. Pridobljeno 4. oktobra 2012.

