Dižveplov monoksid

| |
| |
| Imena | |
|---|---|
| Druga imena
žveplov suboksid
| |
| Identifikatorji | |
| ChemSpider | |
CompTox Dashboard (EPA)
|
|
| Lastnosti | |
| S2O | |
| Molska masa | 80,1294 g/mol[1] |
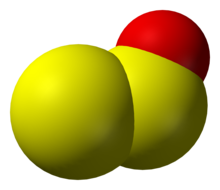
| Videz | brezbarven plin ali temno rdeča trdnina[2] |
| Struktura | |
| Koordinacijska geometrija |
nelinearna |
| Nevarnosti | |
| Glavne nevarnosti | |
| Sorodne snovi | |
| Sorodne snovi | trižveplo žveplov monoksid, ozon, žveplov dioksid |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Dižveplov monoksid ali žveplov suboksid je anorganska spojina s formulo S2O, ki spada med nižje žveplove okside. Je brezbarven plin, ki kondenzira v bledo obarvano, pri sobni temperaturi neobstojno trdnino.[3] Molekula ni linearna. Kot, ki ga oklepajo atomi S-S-O, meri 117,88°. Vez S-S je dolga 188,4 pm, vez S-O pa 146,5 pm.[4]
Sinteza
[uredi | uredi kodo]S2O se lahko pripravi na več načinov. Eden od njih je nepopolno zgorevanje žvepla. Nastane tudi z oksidacijo žvepla z bakrovim(II) oksidom:[5]
- ¾ S8 + 3 CuO → 3 CuS + S2O + SO2
Med druge načine priprave spadata reakcija tionil klorida s srebrovim sulfidom:
- SOCl2 + Ag2S → 2 AgCl + S2O
in termični razpad žveplovega dioksida v razelektritvah.[6]
Raztopina dižveplovega monoksida v ogljikovim tetrakloridu je rumeno obarvana.[5] Trdni S2O se tvori pri temperaturi tekočega dušika. Zaradi nečistoč je pogosto temno obarvan. Med razpadom pri sobni temperaturi nastajajo najprej poližveplovi oksidi in nato SO2.[6]
Sklici
[uredi | uredi kodo]- ↑ 1,0 1,1 1,2 1,3 Disulfur monoxide. NIST. 2008.
- ↑ B Hapke and F Graham (Maj 1989). »Spectral properties of condensed phases of disulfur monoxide, polysulfur oxide, and irradiated sulfur«. Icarus. 79 (1): 47. Bibcode:1989Icar...79...47H. doi:10.1016/0019-1035(89)90107-3.
- ↑ R. Steudel. Sulfur-Rich Oxides SnO and SnO2. Elemental Sulfur und Sulfur-Rich Compounds II, Steudel, R., 2003, Springer, Berlin-Heidelberg. ISBN 9783540449515.
- ↑ D.J. Meschi, R.J. Myers (1959). The microwave spectrum, structure, and dipole moment of disulfur monoxide. Journal of Molecular Spectroscopy 3 (1–6): 405–416. Bibcode: 1959JMoSp...3..405M. doi: 10.1016/0022-2852(59)90036-0.
- ↑ 5,0 5,1 S. R. Satyanarayana, A.R. Vasudeva Murthy (1964). Reactions with Disulphur monoxide Solutions Obtained by the Reduction of Cupric Oxide by Elemental Sulphur (PDF). Proceedings of the Indian Academy of Sciences Section A 59 (4).
- ↑ 6,0 6,1 Cotton in Wilkinson (1966). Advanced Inorganic Chemistry A Comprehensive Treatise. str. 540.
