Izolevcin: Razlika med redakcijama
m Bot: Migracija 44 interwikija/-ev, od zdaj gostuje(-jo) na Wikipodatkih, na d:q484940 |
mBrez povzetka urejanja |
||
| Vrstica 22: | Vrstica 22: | ||
}} |
}} |
||
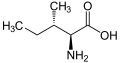
'''Izolevcin''' (okrajšano kot '''Ile''' ali '''I''')<ref>{{cite web | author=IUPAC-IUBMB Joint Commission on Biochemical Nomenclature | title=Nomenclature and Symbolism for Amino Acids and Peptides | work=Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc | url=http://www.chem.qmul.ac.uk/iupac/AminoAcid/ | accessdate=17. 5. 2007}}</ref> je α-[[aminokislina]] s kemijsko formulo HO<sub>2</sub>CCH(NH<sub>2</sub>)CH(CH<sub>3</sub>)CH<sub>2</sub>CH<sub>3</sub>. Izolevcin je [[ |
'''Izolevcin''' (okrajšano kot '''Ile''' ali '''I''')<ref>{{cite web | author=IUPAC-IUBMB Joint Commission on Biochemical Nomenclature | title=Nomenclature and Symbolism for Amino Acids and Peptides | work=Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc | url=http://www.chem.qmul.ac.uk/iupac/AminoAcid/ | accessdate=17. 5. 2007}}</ref> je α-[[aminokislina]] s kemijsko formulo HO<sub>2</sub>CCH(NH<sub>2</sub>)CH(CH<sub>3</sub>)CH<sub>2</sub>CH<sub>3</sub>. Izolevcin je [[esencialna aminokislina]], kar pomeni, da ga človeško telo samo ne more proizvesti, zato ga mora prejemati s hrano. [[Kodoni]], ki zapisujejo izolevcin, so AUU, AUC in AUA. |
||
Izolevcin je zaradi ogljikovodikove stranske verige [[hidrofobnost|hidrofobna]] aminokislina. Poleg [[treonin]]a je izolevcin ena od dveh aminokislin, ki imata v stranski verigi [[kiralni center]]. Možni so 4 [[stereoizomer]]i, vključno z dvema [[diastereoizomer]]oma <small>L</small>-izolevcina. Vendar pa je v naravi prisotna le ena [[enantiomer]]na oblika: (2''S'',3''S'')-2-amino-3-metilpentanojska kislina. |
Izolevcin je zaradi ogljikovodikove stranske verige [[hidrofobnost|hidrofobna]] aminokislina. Poleg [[treonin]]a je izolevcin ena od dveh aminokislin, ki imata v stranski verigi [[kiralni center]]. Možni so 4 [[stereoizomer]]i, vključno z dvema [[diastereoizomer]]oma <small>L</small>-izolevcina. Vendar pa je v naravi prisotna le ena [[enantiomer]]na oblika: (2''S'',3''S'')-2-amino-3-metilpentanojska kislina. |
||
Redakcija: 21:50, 7. april 2016
| |||
| Imena | |||
|---|---|---|---|
| IUPAC ime
Izolevcin
| |||
| Druga imena
2-amino-3-metilpentanojska kislina
| |||
| Identifikatorji | |||
3D model (JSmol)
|
|||
| ECHA InfoCard | 100.000.726 | ||
PubChem CID
|
|||
CompTox Dashboard (EPA)
|
|||
| |||
| Lastnosti | |||
| C6H13NO2 | |||
| Molska masa | 131,18 g·mol−1 | ||
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |||
| Sklici infopolja | |||
Izolevcin (okrajšano kot Ile ali I)[1] je α-aminokislina s kemijsko formulo HO2CCH(NH2)CH(CH3)CH2CH3. Izolevcin je esencialna aminokislina, kar pomeni, da ga človeško telo samo ne more proizvesti, zato ga mora prejemati s hrano. Kodoni, ki zapisujejo izolevcin, so AUU, AUC in AUA.
Izolevcin je zaradi ogljikovodikove stranske verige hidrofobna aminokislina. Poleg treonina je izolevcin ena od dveh aminokislin, ki imata v stranski verigi kiralni center. Možni so 4 stereoizomeri, vključno z dvema diastereoizomeroma L-izolevcina. Vendar pa je v naravi prisotna le ena enantiomerna oblika: (2S,3S)-2-amino-3-metilpentanojska kislina.
Biosinteza
Izolevcin je esencialna aminokislina in ga torej živalski organizmi ne sintetizirajo in ga morajo pridobiti s hrano, predvsem v obliki beljakovin. V rastlinah in mikroorganizmih se sintetizira v več korakih iz piruvične kisline in α-ketoglutarata. Encimi, ki sodelujejo v biosintezi izolevcina, so:[2]
- acetolaktat-sintaza
- acetohidroksikislinska izomeroreduktaza
- dihidroksikislinska dehidrataza
- valin-aminotransferaza
Katabolizem
Izolevcin je glukogena in ketogena aminokislina. Po transaminaciji z α-ketoglutaratom se lahko pretvori bodisi v sukcinil-CoA (ki vstopi v cikel trikarboksilnih kislin, kjer se pretvori v oksaloacetat, slednji pa vstopa v glukoneogenezo) bodisi v acetil-CoA (ki vstopi v cikel trikarboksilnih kislin, kjer pride do kondenzacije z oksaloacetatom in nastaja citrat). Pri sesalcih se acetil-CoA ne more pretvoriti nazaj v ogljikohidrat, temveč se porabi za sintezo ketonskih teles ali maščobnih kislin (zato govorimo, da je izolevcin tudi ketogena aminokislina).
Viri
- ↑ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature. »Nomenclature and Symbolism for Amino Acids and Peptides«. Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc. Pridobljeno 17. maja 2007.
- ↑ Nelson, D. L.; Cox, M. M. »Lehninger, Principles of Biochemistry« 3rd Ed. Worth Publishing: New York, 2000. ISBN 1-57259-153-6.