Fosforjev pentasulfid
| |
| |
| Imena | |
|---|---|
| Druga imena
fosforjev sulfid
žveplov fosfid fosforjev persulfid difosforjev pentasulfid tetrafosforjev dekasulfid | |
| Identifikatorji | |
| ECHA InfoCard | 100.013.858 |
PubChem CID
|
|
| RTECS število |
|
CompTox Dashboard (EPA)
|
|
| Lastnosti | |
| P4S10 | |
| Molska masa | 444.555 g mol |
| Videz | rumena trdna snov |
| Gostota | 2.09 g/cm3 |
| Tališče | 288 °C (561 K) |
| Vrelišče | 514 °C (787 K) |
| hidrolizira | |
| Topnost (v drugih topilih) | 0.222 g / 100g CS2 (pri 17 °C) netopen v C6H6 netopen v vročem kselenu netopen v vročem anisolu. |
| Struktura | |
| Kristalna struktura | triclinic, aP28 |
| Prostorska skupina | P-1, No. 2 |
| Sorodne snovi | |
| Sorodne snovi | P4S3 |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
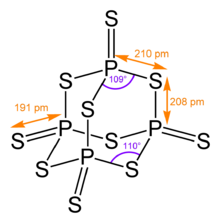
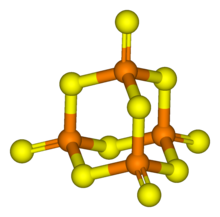
Fosforjev pentasulfid je anorganska spojina, katere molekularna formula je P4S10. Je rumena trdna snov in je ena izmed dveh fosforjevih sulfidov, ki imata tržno vrednost. Zaradi nečistoč se vzorci pogosto pojavljajo v zelenkasto-sivi barvi.
Sestava in sinteza[uredi | uredi kodo]
Njegova tetraedična molekulska struktura je povezana s strukturo admantana in ima skoraj enako strukturo kot fosforjev pentaoksid.[1]
Fosforjev pentasulfid je lahko pridobljen z reakcijo tekočega belega fosforja P4, ki vsebuje žveplo nad 300 °C. Prvo sintezo fosforjevega pentasulfida je leta 1843 [2] po tej metodi prvi uporabil švedski kemik Jöns Jacob Berzelius. Druga možnost, da se oblikuje fosforjev pentasulfid pa je, reakcija elementarnega žvepla ali pirita, FeS2, z ironovim fosfidom, ki vsebuje nečisti Fe2P (je stranski produkt P4 v proizvodnji fosfatovih mineralov) :
- 4 Fe2P + 18 S → P4S10 + 8 FeS
- 4 Fe2P + 18 FeS2 + heat → P4S10 + 26 FeS
Ugotovitve nevarnih lastnosti[uredi | uredi kodo]
Je izjemno škodljiv če se pogoltne ali vdihuje. Hlapi povzročajo draženje oči in dihal. Burno reagira z vodo, ustvarita se vročina in fosforjeva kislina.
Ukrepi za prvo pomoč[uredi | uredi kodo]
- Oči
Ob stiku z očmi takoj izpirajte z vodo vsaj 15 minut, zgornjo in spodnjo veko dvigujte le občasno in takoj poiščite zdravniško pomoč.
- Koža
Ob stiku s kožo takoj odstranite onesnažena oblačila in se temeljito umijte z milom in vodo. Če pride do draženja in ta ostane, takoj poiščite zdravniško pomoč.
- Zaužitje
Ob zaužitju je treba usta takoj izprati z vodo. Ne sme se izzvati bruhanja. Nikoli ne dajajte ničesar v usta nezavestni osebi. Takoj poiščite zdravniško pomoč.
- Vdihavanje
Če pride do vdihavanja, pojdite na svež zrak. Če se pojavi neugodnje pri dihanju in traja, takoj poiščite zdravniško pomoč. Če se je dihanje ustavilo, je treba dati umetno dihanje in takoj poiskati zdravniško pomoč.
- Navodila zdravnikov
Hidrolizira ob pristojnosti vlage v vodikov sulfid in fosforno kislino. Pri vdihavanju je zelo razdražljiv in lahko zahteva umetno dihanje in celo bronhodilator. Sistemski učinki vodikovega sulfida lahko vključujejo spremembe zavesti, mogoče komo, dihalno aretacijo in anoksične krče. Treba je uvesti podporno zdravljenje, še posebej s kisikom ali umetnim dihanjem. Protistrup zaenkrat še ni dokazan.
Ukrepi ob požaru[uredi | uredi kodo]
- Meje vnetljivosti
Ni znano.
- Samovžigna temperatura
V prahu se vžge med 260 in 290 °C.
- Sredstva za gašenje
Za gašenje se uporablja CO2, suha kemikalija, pesek in D aparati z bazo natrijevega klorida po NFRS priporočilih.
- Eksplozijske nevarnosti
Eksplozije lahko povzočijo iskre ali trenje praha, ki predstavlja nevarnost eksplozije. Z zgorevanjem donosi strupene in jedke pline fosforjevega pentoksida in žveplovega dioksida. Reagira z vodo in sprošča strupene in vnetljive pline vodikovega sulfida in fosforno kislino.
- Ukrepi pri gašenju
Pri gašenju ne uporabljajte vode. Celotni ali večji del gradiva je treba prekriti z gasilnim sredstvom za preprečitev ponovnega vžiga. Potrebno je nositi ustrezno zaščitno opremo zaradi strupenih plinov in jedkega dima.
- Plamenišče
Ni znano.
- Eksplozija pri požaru
Ni znano, da je eksploziven.
- Občutljivost na statično razelektritev
Noben.
- Nevarni produkti razkroja
Nastane žveplov dioksid in fosforjev pentoksid pred oksidacijo vodikovega sulfida in fosforne kisline pri reakciji z vodo.
Ukrepi ob nezgodnih izpustih[uredi | uredi kodo]
Ob izpustu je treba nositi ustrezno varovalno opremo. Če pride do razlitja je treba razlitje pokriti, da bi preprečili izpostavljenost vlagi. Prenos samo v čistih in suhih posodat. Potrebno je preprečiti nastajanje prahu. Ko razlitje očistimo je treba sprati vse ostanke na območju razlitja z zelo velikimi količinami vode.
Ravnanje z nevarno snovjo in skladiščenje[uredi | uredi kodo]
Pri ravnanju in uporabi je treba upoštevati proces z nizko vlago v zraku. Ohraniti je treba nizke vlage v ozračju dela področja, na katerih se zabojniki odpirajo in se izdelek prenese na naslednji proces. Izogibajte se drsenju zabojnikov ali grobega ravnanja z njimi. Prah se lahko naelektri s statično elektriko, ki nastane ob mešanju ali drsenju. Upoštevati je treba ustrezne varnostne ukrepe kot so električna ozemljitev, lepljenje in vlago v zraku, kadar se tovor natovori ali raztovori. S tem prepečimo morebitni vžig. Ozemljitev ni potrebna med prevozom.
Hraniti ga je treba v hladnem, suhem in dobro prezračenih prostorih (mehanski prezračevalni izpušni sistem, če je to treba), stran od vnetljivih snovi ali odprtega ognja. Temeljito prezračite vsa dostavna vozila, ali polje avtomobilov za odstranitev plina (vodikovega sulfida). Ozemljitev v shranjevanju ni potrebna.
Nadzor nad izpostavljenostjo[uredi | uredi kodo]
Za zaščito dihal, moramo ob intenzivnejšem ali daljšem izpostavljanju uporabiti dihalni aparat, ki je neodvisen od krožečega zraka, pri manjši izpostavljenosti zadostuje zaščitna maska z visokokakovostnim filtrom delcev. Za zaščito kože uporabimo neprepustna oblačila ( čevlji, rokavice, laboratorijska halja) primerna za preprečitev kontakta s kožo. Za zaščito oči pa uporabimo zaščitna očala, ki dobro tesnijo ali obrazni ščit.
Fizikalne in kemijske lastnosti[uredi | uredi kodo]
Fosforjev pentasulfid se nahaja v trdnem agregatnem stanju. Je rumena praškasta snov, ostrega dražljivega vonja.
Obstojnost in reaktivnost[uredi | uredi kodo]
Fosforjev pentasulfid je treba hraniti pri določenih pogojih. Poizkušamo se izogniti vlagi in nerazdružjivim snovem. Ob stiku z vodo/vlago nastajajo plini in fosforjeva kislina.
Nezdružljiv je z naslednjimi snovmi: vodo, alkoholi in okdidativnimi snovmi.
Pri razkroju nastajajo nevarni produkti kot so: žveplov dioksid in fosforjev pentoksid pred oksidacijo in vodikovim sulfidom in fosforno kislino pri reakciji z vodo.
Toksikološki podatki[uredi | uredi kodo]
Ta izdelek je strupen če ga vdihavamo in načinom izpostavljenosti nad izdelkom. Zmerno draži oči in kožo. Vdihavanje tega izdelka povzroči draženje dihal, oči, kože, nosu, grla in sluznice. Ta produkt lahko hidrolizira vodikov sulfid in fosforno kislino v prisotnosti vlage. Tako vodikov sulfid in fosforna kislina močno dražita oči, kožo in dihalne poti.
Ekotoksikološki podatki / učinki na okolje[uredi | uredi kodo]
- Ni podatka.
Odstranjevanje[uredi | uredi kodo]
Zaradi sulfida imajo te kemikalije, odpadki iz tega izdelka poseben značaj in se štejejo med nevarne odpadke in jih je treba pravilno in ustrezno odstraniti, ob izpolnjevanju vseh zvezni, državnih in lokalnih predpisov.
Transportni podatki[uredi | uredi kodo]
- UN številka: UN1340
- ADR/RID ime: FOSFORJEV PENTASULFID
- ADR/RID razred: 2
- Plakati: nevarno kadar pride v stik z vodo
Podatki o predpisih[uredi | uredi kodo]
| Opozorilni stavki (R) | Obvestilni stavki (S) |
|---|---|
| R35 – Povzroča hude opekline. | S1/2 – Hraniti zaklenjeno izven dosega otrok (v primeru splošne uporabe). |
| S22 – Ne vdihavati prahu. | |
| S26 – Če pride v oči, takoj izprati z obilo vode in poiskati zdravniško pomoč. | |
| S45 – Ob nezgodi ali slabem počutju takoj poiskati zdravniško pomoč (po možnosti pokazati etiketo in embalažo). |
Viri[uredi | uredi kodo]
- ↑ D. E. C. Corbridge (1995). Phosphorus: An Outline of its Chemistry, Biochemistry, and Technology, 5th Edition. Amsterdam: Elsevier. ISBN 0-444-89307-5.
- ↑ Demselben (1843). »Ueber die Verbindungen des Phosphors mit Schwefel«. Annalen der Chemie und Pharmacie. 46: 251. doi:10.1002/jlac.18430460303.
Glej tudi[uredi | uredi kodo]
- varnostni list MSDS
- nevarne snovi
- seznam kemičnih spojin
- kisline
- kemija
- fosfor
- fosforjeve anorganske spojine
Zunanje povezave[uredi | uredi kodo]
- Povezava do datoteke z R in S stavki Arhivirano 2005-03-07 na Wayback Machine.
